Le site des ophtalmologistes de France
Encyclopédie de la vue
Vous êtes ici
Mélanome oculaire
Le mélanome oculaire
Ocular melanoma
Nous remercions beaucoup le Dr Laurence Desjardins (Institut Curie Paris France) qui nous propose le chapitre ci-dessous.
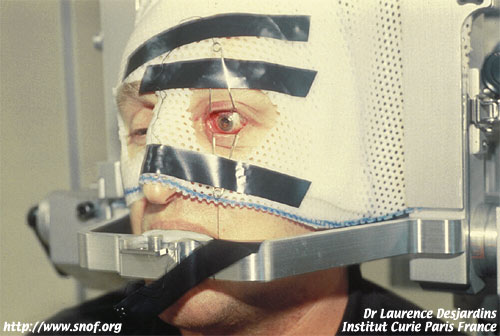
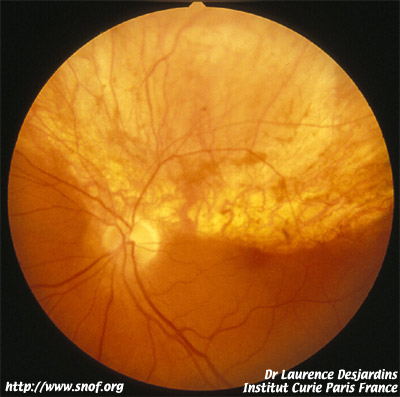
Patient présentant un mélanome oculaire, prêt pour la protonthérapie
Introduction
Le mélanome de l’uvée est la plus fréquente des tumeurs oculaires malignes primitives de l’adulte.
C’est une tumeur relativement rare puisque seulement 500 à 600 nouveaux cas sont diagnostiqués chaque année en France.
Elle se développe préférentiellement dans les yeux bleus ou verts et il est vraisemblable que l’exposition solaire favorise sa survenue. Elle est exceptionnelle chez les sujets de race noire. L’âge moyen au diagnostic est de 56 ans. Bien qu’il ne semble pas s’agir d’une maladie héréditaire, des cas familiaux peuvent se voir ainsi que des associations dans une même famille à des mélanomes cutanés; les formes bilatérales sont très rares. Des études génétiques sont en cours.
La dissémination métastatique survient dans 50% des cas environ parfois plusieurs années après le diagnostic initial. Dans 90 % des cas les métastases sont localisées au niveau du foie.
Le seul traitement de cette tumeur a longtemps été l’énucléation (ou ablation chirurgicale de l’œil) et le syndrome « œil de verre gros foie » est bien connu des gastroentérologues. Depuis une vingtaine d’années les progrès du traitement ont concerné le traitement conservateur de l’œil grâce à l’apparition de nouvelles méthodes de radiothérapie. Les métastases hépatiques lorsqu’elles surviennent gardent un pronostic très péjoratif.
Diagnostic positif
Aspect clinique :
L’aspect extérieur du globe oculaire peut montrer la présence d’un naevus d’Ota. Il s’agit d’une pigmentation unilatérale congénitale bénigne, intéressant la sclère et souvent l’uvée et les paupières. La constatation d’une telle anomalie doit faire pratiquer un examen régulier du fond d’œil car ces patients développent plus souvent que la moyenne des patients des mélanomes de l’uvée.
Une dilatation localisée des vaisseaux épiscléraux peut être en rapport avec une épisclérite mais doit faire rechercher un mélanome du corps ciliaire et ciliochoroïdien dans ce secteur.
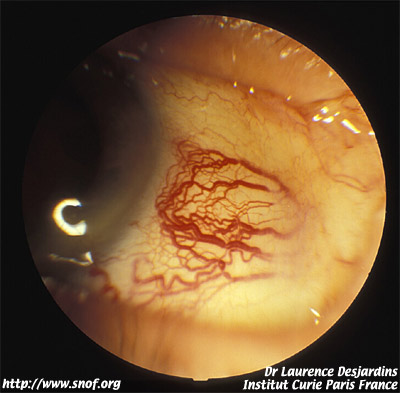
Dilatation des vaisseaux épiscléraux
Dans certains cas c’est l’examen systématique du fond d’œil qui permet le diagnostic du mélanome.
La symptomatologie habituelle des mélanomes de l’uvée est constituée par des troubles visuels qui imposent un examen ophtalmologique avec dilatation et fond d’œil. Lorsque la tumeur commence à refouler la rétine , elle peut entraîner des phosphènes intermittents (éclairs lumineux se répétant toujours au même endroit). En cas d’hémorragie dans le vitré, des myodesopsies ( mouches volantes ) sont présentes.
Le développement de la tumeur au niveau du pôle postérieur de l’œil peut entraîner une baisse d’acuité visuelle. Lorsque la tumeur atteint un certain volume, une amputation du champ visuel est notée.
Enfin les formes évoluées s’accompagnant d’un décollement total de la rétine comportent une perte complète de la vision de l’œil malade. Ces formes évoluées se rencontrent surtout lorsque les symptômes initiaux sont négligés ou mal perçus par le patient , ou lorsque l’examen ophtalmologique est réalisé sans dilatation pupillaire.
L’examen du fond d’œil est un examen capital qui permet le plus souvent le diagnostic.
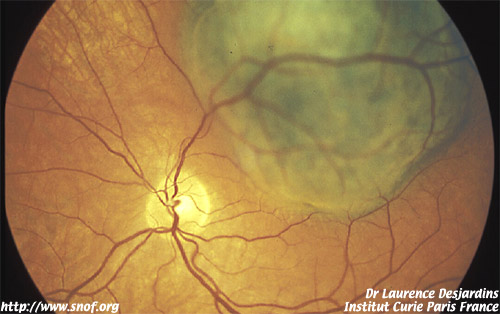
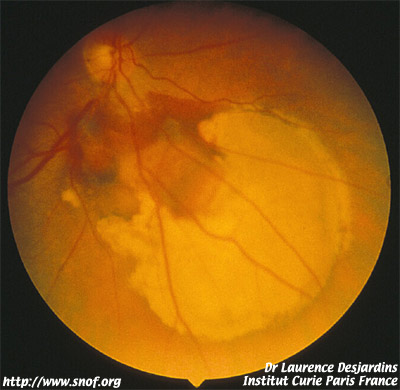
Mélanome de la choroïde
Les mélanomes uvéaux se présentent comme des masse tumorales plus ou moins pigmentées , parfois très noires , parfois au contraires totalement achromes. Du pigment orange peut être visible en surface. Ils peuvent prendre une forme caractéristique en champignon lorsqu’une partie de la tumeur se développe à travers une rupture de la membrane de Bruge vers la cavité vitréenne. Les tumeurs antérieures peuvent parfois envahir la racine de l’iris et la chambre antérieure ou elles deviennent visibles.Les mélanomes de l’iris sont très rares.
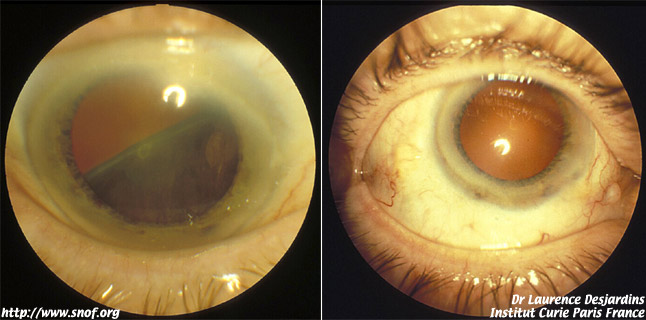
Mélanome ciliaire avant et après traitement
Les examens complémentaires confirment le diagnostic clinique et permettent de documenter la taille de la tumeur.
En angiographie, l’aspect caractéristique du mélanome choroidien réalise un aspect en double réseau dû à la visibilité des vaisseaux intratumoraux sur les clichés précoces. Celui ci n’est visible que dans les tumeurs achromes. Pour les tumeurs fortement pigmentées, seules les modifications rétiniennes de surface sont visibles en angiographie.Les temps précoces sont marqués par un effet masque et on observe une imprégnation progressive inhomogène sur la séquence angiographique. Les pin points sont des petits points hyperfluorescents qui correspondent à des petits décollements séreux localisés.

Mélanome sous-papillaire: angiographie
L’angiographie au vert d’indocyanine met parfois bien en évidence la vascularisation tumorale. Elle est surtout utile en cas de doute diagnostique avec un hémangiome.
En échographie, on a habituellement une échogénéicité élevée en surface avec décroissance rapide de cette échogénéicité. Cette courbe en échographie A est très typique du mélanome choroidien. en échographie B on retrouve l’atténuation des ultras sons souvent responsable d’une excavation choroidienne voire parfois d’une ombre au niveau des tissus orbitaires. L’échographie permet de bien mesurer l’épaisseur de la tumeur.
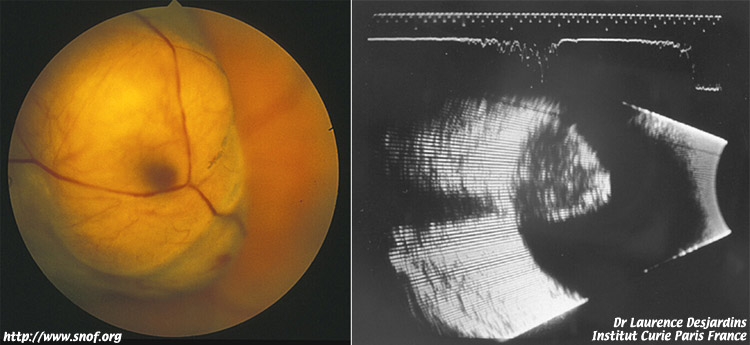
Echographie d'un mélanome
L’IRM montre une image hyperintense en T1 et hypointense en T2 qui s’imprègne après injection de gadolinium.
Au scanner il existe également une prise de contraste après injection Ces examens ne sont indispensables que lorsque l’on soupçonne un envahissement extra scléral ou un envahissement du nerf optique soit lors du bilan initial soit lors de la surveillance d’un mélanome traité par de façon conservatrice.
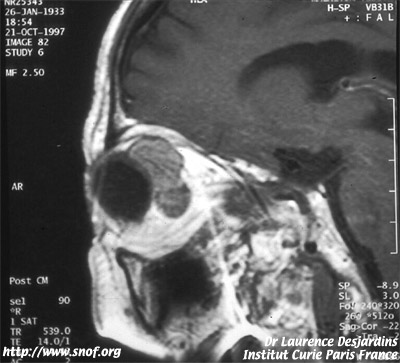
IRM d'un mélanome extrascléral
Une extension extra sclérale de la tumeur peut s’observer en règle dans les tumeurs volumineuses et constitue un facteur de gravité de la maladie et une difficulté thérapeutique supplémentaire.
Plus rarement on peut observer ces extensions extra sclérales sur des tumeurs de plus petit volume.
Les extensions extra sclérales sont suspectées sur l’examen en lampe à fente et l’échographie pour les tumeurs postérieures.Le diagnostic est confirmé par une IRM ou un scanner.
L’examen histologique n’est disponible qu’en cas d’énucléation, d’exérèse chirurgicale de la tumeur ou lorsque une biopsie à l'aiguille est pratiquée avant le traitement conservateur de la tumeur (doute diagnostique).
Actuellement la plupart des traitements conservateurs radiothérapiques sont pratiqués sans examen histologique préalable.
Après une énucléation l’examen histologique précise le type histologique de la tumeur. l’existence ou non d’un envahissement scléral , extra scléral ou du nerf optique et l’aspect de la vascularisation tumorale.
Les formes histologiques du mélanome choroidien sont décrites dans la classification de Callender puis plus récemment dans celle de MC Lean.
On distingue :
- Les formes fusiformes A et B de bon pronostic (cellules fusiformes à noyau ovalaire)
- Les formes épithélioides de mauvais pronostic (cellules de grande taille , rondes à noyau arrondi contenant 1 à 2 nucléoles)
- Les formes mixtes ( mélange de cellules fusiformes et épithélioides). Le pronostic dépend du pourcentage de cellules épithélioides avec un pronostic péjoratif si celui-ci dépasse 50%.
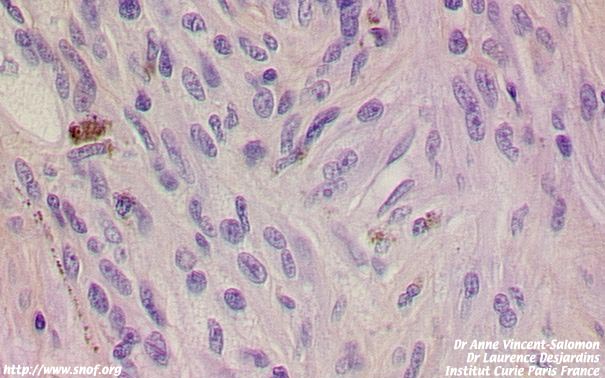
Mélanome de type fusiforme
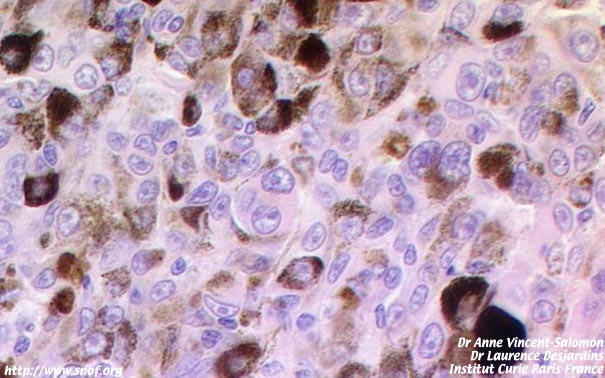
Mélanome de type épithélioïde
L’extension en profondeur de la tumeur est importante à préciser. L’extension intra sclérale est fréquemment retrouvée lors des énucléations pour de volumineux mélanomes : elle ne nécessite pas de traitement particulier.
Le franchissement scléral avec survenue d’une extension extra sclérale (donc orbitaire) justifie pour nous une irradiation complémentaire.
L’examen histologique permet en outre d’étudier la densité et le type de la vascularisation tumorale qui a une valeur pronostique avec en particulier un caractère péjoratif pour la formation de boucles et de réseaux vasculaires.
L’examen histologique peut être d’interprétation difficile après irradiation : il persiste souvent alors une masse cicatricielle dont il est impossible d’affirmer le caractère actif ou inactif. on peut s’aider dans ce cas des techniques immunohistochimiques en particulier avec l’anticorps monoclonal Ki67 qui montrent la diminution de l’activité mitotique de la tumeur.
Actuellement on réalise le plus souvent chaque fois que l’on dispose de tissu tumoral des analyses chromosomiques de la tumeur : Les anomalies retrouvées dans le mélanome choroidien sont surtout la monosomie 3 et la multiplication du 8. Des études récentes ont montré qu’il existait un lien entre ces anomalies et le pronostic vital du patient.
Diagnostic différentiel
Autres lésions pigmentées du fond d’œil :
Les naevi :
L’un des problèmes les plus difficiles est de différencier les naevi suspects des mélanomes choroïdiens.
Les naevi bénins sont des lésions pigmentées de la choroïde fréquentes (retrouvées chez 6 à 10 % des patients) qui lorsqu’elles sont typiques, ne posent pas de problème diagnostique. Ils sont de petite taille (1 à 5 mm de diamètre), plans ou très peu saillants, asymptomatiques, et souvent parsemés de druses qui témoignent de l’ancienneté de leur présence. Ils ne nécessitent qu’un contrôle annuel du fond d’œil. Le problème est plus difficile avec les naevi suspects. On considère qu’un naevus est suspect lorsque l’un au moins des éléments suivants est présent :
- Existence de troubles visuels récents (scotome, métamorphopsies, myodésopsies, etc.)
- Décollement séreux de la rétine
- Epaisseur supérieure à 2 mm
- Diamètre supérieur à 7 mm
Lorsque l’on a affaire à un naevus suspect, une surveillance beaucoup plus rapprochée doit être instituée et en cas de croissance documentée, on considère qu’il s’agit en fait d’un mélanome débutant et un traitement radiothérapique est pratiqué.. Le suivi est primordial car il n’y a aucun examen complémentaire capable de différencier de façon formelle un naevus suspect d’un petit mélanome débutant. La surveillance devra être prolongée car certaines lésions peuvent rester quiescentes pendant plusieurs années et se mettre brusquement à évoluer.
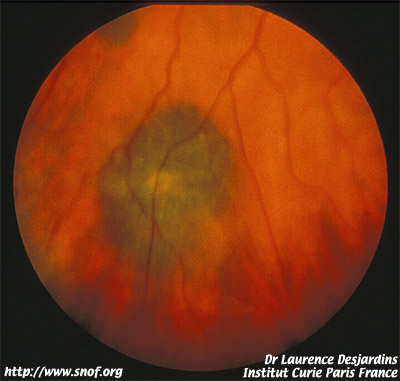
Naevus de la choroïde
Les mélanocytomes de la papille ne nécessitent qu’une simple surveillance. Ils sont en général de diagnostic facile. Ce sont des lésions péripapillaires souvent très pigmentées, en règle non évolutives Néanmoins, certains de ces mélanocytomes peuvent grossir très lentement et entraîner des déficits du champ visuel La dégénérescence maligne est exceptionnelle.
Les autres lésions pigmentées du fond d’œil qui sont des lésions de l’épithélium pigmentaire (hamartome combiné de la papille et de l’épithélium pigmenté, hyperplasie congénitale bénigne , adénomes de l’épithélium pigmentaire) sont moins fréquentes et ne posent en général pas de problème diagnostique.
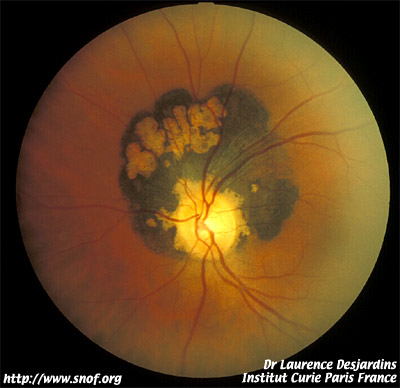 Hypertrophie de l'épithélium pigmenté |
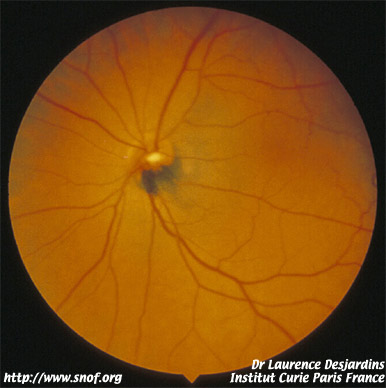 Mélanocytome |
Hypertrophie de l'épithélium pigmenté
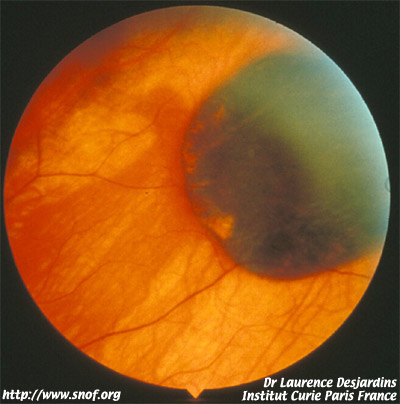
Les hémangiomes choroïdiens :
Ils peuvent être confondus avec des mélanomes achromes bien que leur aspect clinique soit en général bien particulier. Ils se présentent sous forme de masse choroïdienne de coloration rouge orangée comme le reste de la rétine, souvent proches du pôle postérieur.
Lorsque la tumeur fait plus de 3 mm d’épaisseur, l’échographie B permet aisément de la différencier d’un mélanome choroïdien en montrant une masse globalement hyperéchogène sans atténuation des ultrasons et sans excavation choroïdienne.
En cas de doute, l’angiographie au vert d’Indocyanine permet de trancher en montrant un aspect caractéristique des hémangiomes : hyperfluorescence homogène majeure d’apparition précoce avec hypofluorescence tardive.
Hémangiome choroïdien
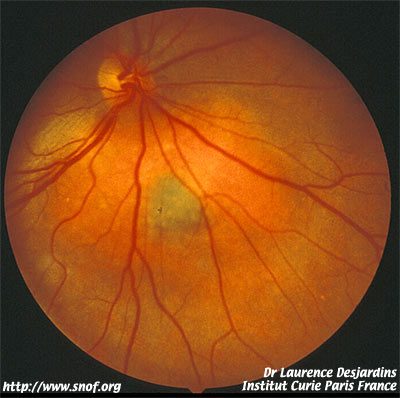
Les métastases choroïdiennes :
Elles sont de diagnostic facile lorsqu’elles surviennent dans un contexte de maladie cancéreuse disséminée, lorsqu’elles sont multiples ou bilatérales. Néanmoins, les métastases peuvent être uniques et révélatrices de la maladie et dans ce cas poser un problème diagnostic avec les mélanomes achromes. La forme des métastases est en général différente. Ce sont des lésions plutôt infiltrantes, plus larges que hautes, souvent rapidement évolutives et entraînant vite un décollement rétinien important. Elles ne sont pratiquement jamais en forme de champignon.
L’échographie montre des lésions dont l’échogénéicité est plutôt homogène contrairement à ce que l’on observe dans les mélanomes.
L’IRM permet de rechercher des lésions cérébrales associées mais a souvent bien du mal à différencier une métastase unique et saillante d’un mélanome achrome. En cas de doute, on peut réaliser un bilan général à la recherche d’un cancer primitif. Les causes les plus fréquentes de métastase oculaire sont le cancer du sein chez la femme et le cancer du poumon chez l’homme. On peut donc demander une mammographie et un scanner thoracique en complétant éventuellement par une échographie abdominale et un examen ORL. Dans la plupart des cas, la découverte d’un cancer primitif permet d’affirmer le diagnostic de métastase choroïdienne.
Les métastases choroïdiennes des mélanomes cutanés peuvent également être trompeuses du fait de leur pigmentation. L’interrogatoire est là essentiel en retrouvant le plus souvent l’antécédent de mélanome cutané mais quelquefois la métastase est révélatrice d’une tumeur cutanée passée inaperçue.
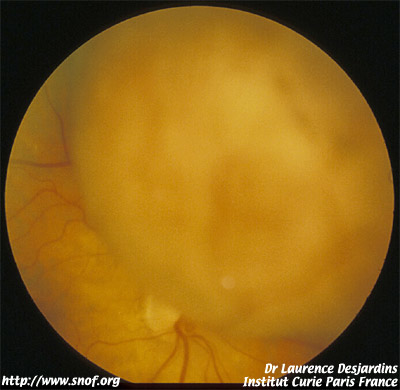
Métastase choroïdienne
Les ostéomes choroïdiens :
Ce sont des lésions habituellement juxtapapillaires, apparaissant en règle chez femmes jeunes, uni ou bilatérales et correspondant à des ossifications de la choroïde.
L’aspect au fond d’œil est en général celui de plages jaunâtres ou orangées, planes avec des altérations de l’épithélium pigmentaire aboutissant souvent à des zones d’hyperplasie qui peuvent orienter à tort vers un mélanome.
Les ostéomes choroïdiens peuvent augmenter de volume lentement et être responsables de néovascularisation choroïdienne avec décollement séreux de la rétine et baisse d’acuité visuelle. Les examens complémentaires peuvent aider au diagnostic ( angiographie et échographie ).
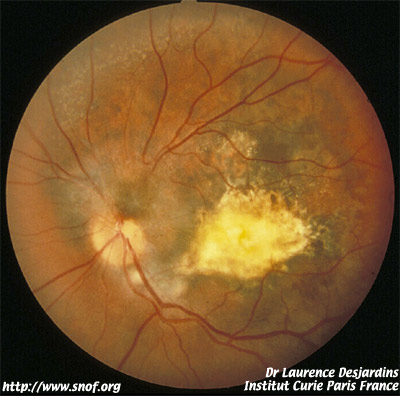
Ostéome choroïdien
Les hématomes choroïdiens :
L’une des causes les plus importantes d’erreur diagnostique est représentée par les hématomes choroïdiens. Ceux-ci sont le plus souvent en rapport avec une néovascularisation choroïdienne liée à l’âge et siègent habituellement dans la région maculaire mais peuvent également être excentrés. La membrane néovasculaire est responsable d’un saignement derrière l’épithélium pigmentaire aboutissant à un hématome choroïdien qui peut ressembler à une tumeur choroïdienne pigmentée. Si la lésion est maculaire, il peut être utile d’examiner le fond d’œil controlatéral qui montre souvent une dégénérescence maculaire ou des druses.
Hématome dû à une DMLA
Les sclérites postérieures :
Ce sont des lésions rares, plus fréquentes chez les femmes, qui posent de réels problèmes diagnostiques, car elles peuvent fortement ressembler à un mélanome achrome. Le diagnostic est plus facile lorsqu’il existe des signes inflammatoires mais ceux-ci peuvent être absents. Il faut rechercher des douleurs lors des mouvements de l’œil, une papillite, une uvéite antérieure. Des plis choroïdiens peuvent être présents. A l’échographie B, la sclérite entraîne souvent une visibilité anormale de la sclère. Le bilan étiologique doit rechercher les causes habituelles des uvéites (arthrite rhumatoïde, sarcoïdose...)
Le pronostic vital
La mortalité des mélanomes choroidiens a été beaucoup étudiée après énucléation. Elle est d’environ 30% à 5 ans et 50 % à 10 ans. Les principaux facteurs pronostiques sont le type histologique de la tumeur, son plus grand diamètre, l’âge du patient avec un pronostic plus péjoratif pour un âge supérieur à 60 ans au diagnostic, et la localisation de la tumeur avec un pronostic plus péjoratif pour les tumeurs antérieures.
L’existence d’une extension extra sclérale est également un facteur de mauvais pronostic. Plus récemment d’autres facteurs de risque métastatique ont été mis en évidence (présence de boucles vasculaires en histologie , monosomie 3) ou sont à l’étude (recherche de cellules circulantes). De nombreuses études rétrospectives n’ont pas mis en évidence de différence significative de pronostic vital entre l’énucléation et les traitements conservateurs radiothérapiques pour des tumeurs de taille comparables. Une étude randomisée a été faite aux Etats-Unis ( COMS : collaborative ocular melanoma study ) qui a démontré l’absence de différence significative entre énucléation et irradiation par disque d’iode 125 pour des tumeurs de taille moyenne.
Traitement
Le seul traitement disponible pour le mélanome choroidien a longtemps été l’énucléation. les premiers traitements conservateurs ont été réalisés dans les années 50 par Stallard qui utilisa la curietherapie par des plaques de cobalt 60. Ces traitements conservateurs ont longtemps été réservés aux patients monophtalmes.
Puis Zimmerman en 1978 a souligné que l’énucléation n’évitait pas toujours la survenue d’une dissémination métastatique. La curietherapie au cobalt 60 a progressivement été remplacée par la curietherapie au ruthénium qui émet un rayonnement béta peu pénétrant ( actif seulement sur les tumeurs peu épaisses ) et surtout par la curietherapie à l’iode 125 que nous utilisons à l’institut Curie. L’irradiation par faisceau de protons qui permet une irradiation homogène de la tumeur existe depuis 1975 à Boston et en France à Orsay et à Nice depuis 1991.
Les méthodes thérapeutiques
L’énucléation
L’ablation chirurgicale de l’œil est une intervention mutilante actuellement réservée aux tumeurs massives.
Elle sera si possible suivie de la mise en place d’un implant intra orbitaire sur lequel seront greffés les muscles oculomoteurs afin d’assurer un aspect esthétique satisfaisant et une bonne motilité de la prothèse
L’examen anatomopathologique est essentiel.Il précise le type histologique (fusiforme, épithélioide ou mixte) et l’extension locorégionale. Des fragments tumoraux sont prélevés pour l’étude cytogénétique et immunologique de la tumeur.En cas d’extension extra sclérale une radiothérapie orbitaire complémentaire est indispensable.
La protonthérapie
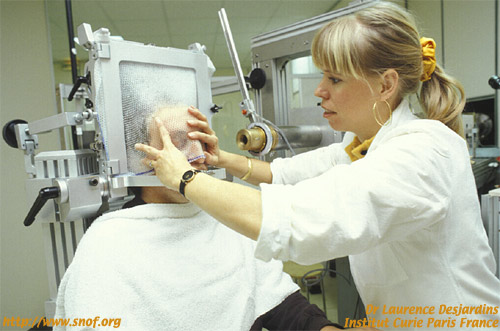
Elle consiste à irradier la tumeur par un faisceau de protons accélérés.
L’irradiation elle même est précédée d’un repérage chirurgical de la tumeur avec mise en place de clips de tantale qui sont suturés sur la sclère.Les données recueillies lors de l’intervention et lors du bilan pré opératoire( échographie, angiographie, photographies, biométrie) sont introduites dans un programme informatique..On détermine ensuite la position idéale de l’œil pendant le traitement ainsi que les doses reçues par la tumeur et par chacune des structures oculaires. On délivre à la tumeur une dose de 60 grays équivalents cobalt en 4 fractions et 4 jours. Une marge de sécurité de 2,5 mm autour de la tumeur est incluse dans le champ d’irradiation.
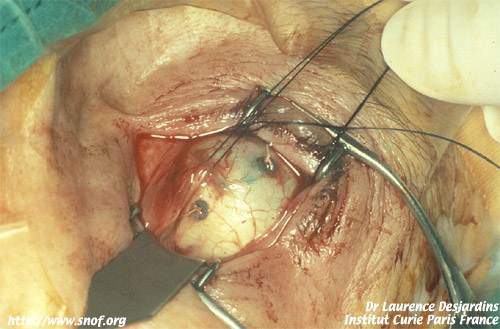
Pose des clips de tantale
Plusieurs milliers de patients ont étés traités par protonthérapie pour un mélanome oculaire dans le monde.
Les résultats à long terme montrent un contrôle tumoral supérieur à 95 % avec un taux d’énucléation secondaire de l’ordre de 10%. Il existe une corrélation nette entre le volume tumoral et la fréquence des complications oculaires( glaucome, cataracte, décollement de rétine, inflammation).
La localisation de la tumeur est également importante pour le résultat visuel. Après 5 ans d’évolution environ 50 % des patients gardent une acuité visuelle supérieure ou égale à 1/10.

Chaise robotisée
La curiethérapie
Elle consiste à irradier la tumeur à l’aide d’une plaque suturée à la sclère contenant habituellement soit du ruthénium soit de l’iode 125.
Le cobalt n’est plus guère utilisé actuellement. A l’institut Curie nous utilisons de l’iode 125 qui émet un rayonnement gamma de faible énergie. De ce fait le rayonnement est totalement arrêté par un métal lourd tel que l’or. Les grains d’iode ont une demie vie de 60 jours et doivent être renouvelés fréquemment. Ils sont disposés dans des disques en or de taille variable ce qui permet d’avoir une irradiation nulle au niveau des paupières de la glande lacrymale et de l’orbite.
Une dose de 90 grays est délivrée au sommet. La source radioactive étant localisée au niveau de la sclère il existe un surdosage à la base qui est d’autant plus important que la tumeur est plus épaisse.C’est pourquoi il vaut mieux éviter de traiter par disque les tumeurs trop épaisses, postérieures ou à cheval sur l’équateur pour ne pas irradier inutilement le pole post de l’œil.
Pour les tumeurs antérieures à l’équateur les résultats obtenus avec les disques d’iode 125 sont très satisfaisants avec un contrôle tumoral supérieur à 95 % et un taux de complications très faible ( la complication la plus fréquente étant la cataracte).
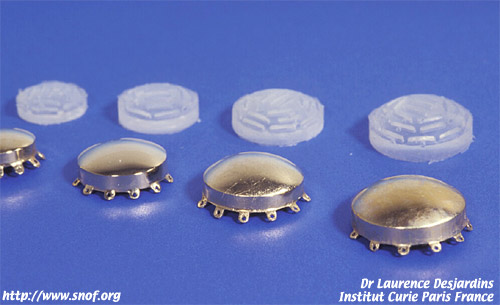
Disques d'iode 125
L’exérèse chirurgicale
L’exérèse chirurgicale de la tumeur est parfois possible en conservant le globe oculaire pour des tumeurs à base étroite. On réalise sous hypotension contrôlée et après vitrectomie une dissection lamellaire de la sclère avec exérèse de la tumeur en bloc. Le patient doit être en bon état général pour supporter une anesthésie générale prolongée avec hypotension, ce qui limite les indications de ce traitement.
La thermothérapie
Il s’agit d’une méthode récemment développée qui consiste à traiter la tumeur à l’aide d’un laser diode.
Ce laser émet dans le rouge à 810 nm et est absorbé par les tissus pigmentés. Il permettrait de détruire le mélanome sur 2 ou 3 mm d’épaisseur mais ne serait pas actif sur les cellules intra sclérales. Les résultats de ce traitement montrent un taux de récidive élevé autour de 30 % et il paraît préférable d’utiliser un traitement par irradiation.
Les indications thérapeutiques
L’énucléation reste indiquée pour les tumeurs très volumineuses ( épaisseur supérieure à12mm ou diamètre supérieur à 20 mm) et se discute en cas d’extension extra sclérale ou d’envahissement du nerf optique.
Les tumeurs postérieures ou à cheval sur l’équateur et les tumeurs antérieures de plus de 5mm d’épaisseur relèvent plutôt d’une protonthérapie (sauf les volumineuses tumeurs antérieures supéro externe qui sont mieux traitées par disque d’iode 125 afin d’éviter l’irradiation de la glande lacrymale et la sécheresse de l’œil).
Les petites tumeurs antérieures sont mieux traitées par disque d’iode (sauf les tumeurs iriennes qui relèvent plutôt d’une protonthérapie pour diminuer la dose à la cornée).
Dans certains cas particuliers (tumeurs épaisse à base plutôt étroite, sujet jeune, doute quand à la nature de la lésion) on peut proposer une exérèse chirurgicale.
 Mélanome avant traitement |
 Mélanome après traitement |
Le suivi post thérapeutique
Il doit être prolongé et rigoureux.
Après un traitement conservateur, il doit comporter un examen ophtalmologique tous les trois mois pendant deux ans puis tous les 6 mois avec échographie de l’œil tous les six mois.
En cas de survenue de métastases hépatiques il est important de diagnostiquer les lésions hépatiques le plus précocément possible en insistant auprès du patient pour qu’il maintienne un contrôle de l’échographie hépatique tous les six mois pendant 10 ans.
Le traitement est alors pris en charge par les chirurgiens et les oncologues. Un bilan précis doit être réalisé avec scanner hépatique et groupage HLA. Si une exérèse chirurgicale de la métastase est possible , celle ci est réalisée et donne les survies les plus prolongées. On peut profiter de l’intervention pour mettre en place un cathéter dans l’artère hépatique.
En cas de métastases multiples ou plus diffuses on peut proposer une chimiothérapie soit par voie intraveineuse soit directement dans l’artère hépatique. Les drogues les plus actives sont le déticène et la fotemustine. Plus récemment on a proposé pour les patients HLA A2 (dont les tumeurs sont porteuses des antigènes en surface) une vaccination par des peptides spécifiques du mélanome choroidien. ( peptide NA 17 ). Ce protocole est en cours d’étude.
Pour les tumeurs volumineuses de mauvais pronostic il serait souhaitable de trouver une thérapeutique adjuvante pour prévenir l’apparition des métastases. Un protocole de traitement adjuvant par le déticène n’a pas montré de bénéfice statistiquement significatif pour les sujets traités. Une étude de l’efficacité de l’immunisation par les peptides NA17 est proposée.
Conclusion
Le mélanome choroidien reste une maladie grave qui met en jeu le pronostic visuel de l’œil atteint et le pronostic vital.
Le dépistage précoce améliore considérablement le pronostic. Il est donc important d’examiner soigneusement le fond d’œil après dilatation pupillaire dès qu’il existe une symptomatologie visuelle.