Embryologie de l'oeil
Nous tenons à remercier chaleureusement les personnes qui ont accepté de nous aider dans la réalisation de ce chapitre, et particulièrement:
- le Professeur Jacques-Patrick Barbet, Laboratoire d'histologie, embryologie et cytogénétique, Faculté de Médecine Cochin Port-Royal Paris France
- le Professeur Patrick Calvas, Chef du Service de Génétique CHU Toulouse-Purpan, France
- le Docteur Christian Hamel Directeur de Recherches Responsable équipe génétique Inserm U. 254 Montpellier France
- M. Simon Saule, Directeur de recherche UMR 146 CNRS/IC Différenciation cellulaire et moléculaire, Faculté d'Orsay France
Nous ne présentons qu'un survol d'une discipline très complexe. En parcourant la génétique et la biologie moléculaire nous rencontrerons plusieurs prix Nobel, et nous décrirons les derniers progrès de la génétique moderne.
L'embryologie de l'oeil présente de multiples intérêts. En effet, l'oeil est un organe facilement accessible, formé par le cerveau et le revêtement ectodermique. Par ailleurs il se prête bien aux expérimentations animales. La génétique de son développement commence à être très partiellement comprise et ouvre de nombreuses voies derecherche (cellules souches, transdifférenciation).
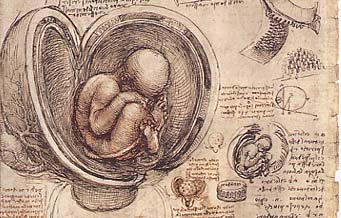
Historique de l'embryologie de l'oeil
L'embryologie a été étudiée par différents chercheurs, mais nous n'évoquerons que des personnages célèbres:
-
Léonard de Vinci, le précurseur
-
Ida Mann, la référence mondiale en embryologie oculaire
-
Van Duyse Historien et anatomiste belge
-
Hans Spemann Prix Nobel de Médecine en 1935
1) Introduction
L'embryologie est étroitement liée à la génétique qui étudie le fonctionnement des gènes, et à la biologie moléculaire qui s'intéresse aux cellules et à leur devenir.
On va dire que tout a commencé avec Léonard de Vinci qui eut du mal à faire accepter à ses contemporains de lui laisser examiner un foetus. C'étaient les débuts de l'embryologie descriptive.
Ce n'est que bien plus tard, en 1866 que Mendel découvrit les lois de l'hérédité mais ces informations furent surtout redécouvertes en 1900.
La théorie chromosomique fut établie par Morgan qui comprit que les gènes étaient localisés sur les chromosomes. C'est lui qui utilisa la mouche du vinaigre Drosophila melanogaster pour étudier la génétique parce que cette mouche n'a que 4 paires de chromosomes, et que la femelle pond des centaines d'oeufs tous les neufs jours.
C'est avec Sturtevans que Morgan va établir les premières cartes génétiques en précisant l'emplacement de certains gènes. Cela va permettre à Morgan d'obtenir le prixNobel de physiologie et de médecine en 1933.
Darwin étudia l'Evolution et, dans son livre "L'origine des espèces", et il pensait que ce sont des modifications progressives des espèces d'animaux qui vont entraîner l'apparition de nouvelles espèces.
Enfin, Watson et Crick découvrirent la structure en double hélice de l'ADN, ce qui leur valut le Prix Nobel de médecine en 1962.
Tous ces personnages fameux ont contribué à la compréhension de l'hérédité et du développement des organismes au cours des différents stades de l'embryologie, mais il faut savoir qu'il reste encore aujourd'hui beaucoup de mystères et d'inconnu. Ces points d'interrogation apparaissent dès qu'on évoque l'évolution des espèces (la phylogénèse) ou le développement de l'individu (l'ontogénèse).
2) Léonard de Vinci

Le précurseur fut Léonard de Vinci qui, dès les années 1500, étudia l'embryologie humaine ainsi que la cardiologie. Il essayait d'étudier "l'âme [...] de la mère qui commence par construire dans la matrice la forme de l'Homme". Il concevait l'esprit de la mère comme la source du développement du foetus.
Il comprenait que "l'enfant [...] tire vie et subsistance de la vie et de l'alimentation maternelle [...] et une âme unique gouverne les deux corps".
Il étudia précisément les organes féminins et les foetus dans les années 1510-1512, et l'on pense que c'est dans cette période qu'il obtint un foetus de 7 mois qu'il utilisa pour les dissections et l'étude anatomique.
3) Ida Mann (1893-1983)

Ida Mann 1925
Dame Ida Mann fut une pionnière dans l'étude de l'embryologie de l'oeil et utilisa son énergie pour développer l'ophtalmologie durant de nombreuses décennies. Cette femme dynamique naquit à Londres en 1893. Sa biographie commence par "I don't remember being born...".
Ses ancêtres maternels étaient meuniers et fermiers. L'un de ses oncles émigra en Australie en 1880, ce qui la rapprochera plus tard de ce pays.
Sa scolarité se déroula à West Hampstead. L'élève était douée et curieuse de tout. Son père tenait à ce qu'elle travaillât et l'a fit embaucher deux ans dans l'administration postale dans laquelle il était employé.
Mais son but était de réaliser des études universitaires et elle commença à étudier dans la seule Université accessible aux femmes, the London School of Medicine for Women fondée en 1874. Elle fut enrôlée en 1914, au début de la guerre, et alla travailler à l'hôpital St Mary où elle termina ses études en 1920.
Elle fut attirée par l'enseignement du Professeur Frazer qui étudiait l'embryologie et possédait une collection célèbre d'embryons humains. Il lui disait souvent "Don't believe the books; go and look for yourself" (Ne crois pas les livres; va et explore toi-même).
En 1920 elle participa aux cours du Professeur Vogt à Zurich qui avait organisé un enseignement en allemand, français et anglais. L'année suivante, en 1921, elle rencontra le Professeur Axenfeld qui opérait les cataractes avec juste une anesthésie topique par collyre à la cocaïne. Son parcours l'amena à voir le Professeur Jules Gonin à Lausanne qui excellait en chirurgie rétinienne.
En 1925 elle obtint un poste de chirurgien assistante au Central London Ophthalmic Hospital, puis en 1927, au Moorfields Eye Hospital et en 1928 au Royal Free Hospital.
Elle écrivit The Development of the Human Eye (1928, 1949,1950 & 1964) et Developmental Abnormalities of the Eye (Cambridge 1937, 2nd ed.London 1957)
Elle tenait toujours à dessiner elle-même les illustrations de ses livres :
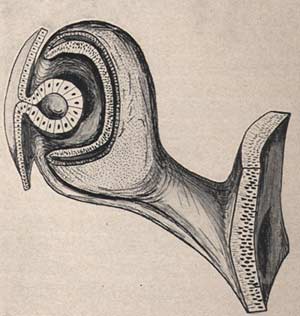
Development of the human eye
Ida Mann 1928
A la fin de la deuxième guerre, en 1939, associée au pathologiste Davidine Pullinger, elle étudia les effets du gaz moutarde sur les yeux Sa carrière se poursuivit et lui permit d'obtenir de nombreuses distinctions ( le Gifford Edmonds Prize en 1927, the Harrison Gale Lecture in 1929, le Doyne Memorial Lecture en 1928, le Nettleship Lecture en 1932, et le Montgomery Lecture en 1935).
En 1942 elle devint professeur à l'Université d'Oxford. Elle consultait alors et travaillait au Oxford Eye Hospital et au Nuffield Laboratory of Ophthalmology. En 1944 elle se maria avec le professeur William Ewart Gye, directeur de l'Imperial Cancer Institute de Londres.
Elle étudia les carences vitaminiques et leurs incidences sur la vision de l'avitaminose A. Son intérêt pour de nombreux sujets se retrouve dans ses publications sur l'insuffisance de convergence, les lentilles cornéennes, les thyrotoxicoses ou son fameux livre "The Science of Seeing" en 1946. Il s'opposait au livre "Art of Seeing" d'Aldous Huxley.
Ida Mann raconte dans sa biographie comment elle opérait les animaux du zoo de cataracte, tentait d'équiper un singe albinos avec des lunettes ou plaçait une prothèse oculaire à un énorme python.
En 1945 elle devint Senior Surgeon au Moorfields Eye Hospital, et elle fut la première femme à occuper un tel poste.
Accompagnée de son mari, elle partit en Australie en 1949, embauché par le Royal Perth Hospital. Elle alla étudier l'incidence du trachome chez les aborigènes du nord du pays et pendant dix ans s'occupa de ces populations. Elle décrivit les pathologies locales, la prévalence du trachome qu'on croyait éteint.
Elle continua à travailler par la suite en Papouasie Nouvelle Guinée et à Taiwan; ces longs voyages et son expérience lui permirent d'écrire Culture, Race, Climate and Eye Disease en 1966. Elle explora aussi l'Inde et l'Afrique du Sud.
Consultante pour l'OMS, elle parcourut le monde et participa à la fondation de la Society of Geographic Ophthalmology. Sa connaissance et son expérience lui permirent d'écrire The Cockney and the Crocodile et China 13 sous son nom d'épouse, Caroline Gye.
En 1980 elle fut élevée à l'ordre de Dame of the British Empire (DBE) et fut couverte d'honneurs.
Ida Mann continua à pratiquer l'ophtalmologie jusqu'à ce qu'elle ait 85 ans ! Nous ne pouvons qu'engager le lecteur à lire au moins sa biographie The Chase, Fremantle Arts Centre Press 1983, qui révèle un auteur plein d'humour, d'humilité et de charme.
Elle termine sa vie en repensant à ce qu'elle écrivait déjà en 1910 :
"Now have I done that which I set out to do, and now I am happy -- for a day".

4) Daniel Van Duyse (1852-1924)
Nous trouvons en Belgique le Professeur Van Duyse, né en 1852 à Gand, et mort à Bruxelles en 1924.

Eléments d'embryologie et de tératologie de l'oeil
Daniel Van Duyse 1904
Jean-Paul Wayenborgh nous rappelle que Van Duyse était le fils du poète Prudens Van Duyse, appartenant au mouvement flamant. Il avait trois frères connus, le musicologue Florimond, l'écrivain Gustave et l'archéologue Herman.
Daniel obtint son doctorat à l'Université de Gand en 1876. Il se spécialisa en ophtalmologie à Paris de 1877 à 1881, avec Panas, Wecker, Galezowski, Abadie, Landolt, et àVienne avec von Arlt, Fuchs, von Jaeger, Stellwag von Carion et Mauthner, à Londres avec Critchett, Bader et Nettelship, à Berlin avec J. Hirschberg et à Heidelbergavec 0.Becker.
Il se spécialisa encore à Strasbourg, en 1883, avec von Recklinghausen.
Il travailla comme professeur d'anatomie pathologique à l'Université de Ghent en 1891 et comme professeur d'ophtalmologie en 1899. Il devint le spécialiste des anomalies congénitales de l'oeil (tératologie) et publia de nombreux textes sur les malformations palpébrales, les kystes dermoïdes, les malformations du nerf optique, l'aniridie, la persistance de la membrane pupillaire, les colobomes maculaires, l'anophtalmie, la cryptophtalmie, la cyclopie, les kystes colobomateux...
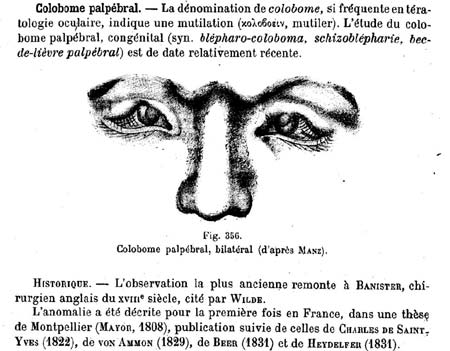
Professeur Van Duyse
Etude des colobomes 1904
Il était aussi spécialiste d'histopathologie de l'oeil et de l'orbite, particulièrement des angiomes.
Il publia beaucoup sur l'utilisation de la pilocarpine, la radiothérapie, l'endophtalmie traumatique et la chirurgie anti glaucomateuse.
Il était aussi intéressé par l'Histoire de la Médecine et écrivit sur Michel Brisseau, les fameux oculistes du XVIIIe siècle, les prothèses oculaires dans l'Antiquité...
Il publia Coup d'oeil sur l'Histoire de l'Ophtalmologie en Belgique au XIXe siècle, en 1912. Il fut l'auteur des chapitres sur l'embryologie et la tératologie de l'oeil dans la première "Encyclopédie française d'Ophtalmologie" publié par Lagrange et Valude, et republiée en tant que monographie : "Eléments d'embryologie et de tératologie de l'oeil" Paris 1904.
Il fut un membre fondateur de la Société Belge d'Ophtalmologie et fut son secrétaire jusqu'à sa mort, en 1924.
5) Hans Spemann (1869-1941)

Hans Spemann
Ce biologiste allemand obtint le prix Nobel de physiologie-médecine en 1935 pour ses travaux sur l'induction embryonnaire au niveau des organes.
En 1902 il montra que lorsqu'on sépare deux cellules d'un embryon de salamandre, on voit naître deux têtards qui donneront des animaux normaux. Cela alla à l'en contre de la théorie de Weismann (1885) qui disait (à tort) que le contenu génétique d'une cellule diminuait au fur et à mesure qu'elle se différenciait..
A partir de 1902 il fit des expériences d'induction sur les yeux de grenouilles. Il étudia les phénomènes d'induction et de spécialisation. Il étudia surtout le développement du cristallin et de la vésicule optique chez la grenouille. Il expliquait que la formation de l'oeil et du cristallin était sous la dépendance du cerveau et qu'ils n'apparaissaient pas si cette zone était cautérisée. Il démontrait aussi que la formation du cristallin nécessitait le contact de la vésicule optique et de l'ectoderme.
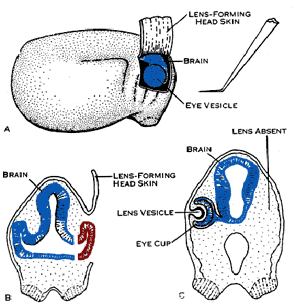
Il révéla en 1921 le rôle inducteur de la lèvre supérieure du blastopore de la gastrula chez le triton. Il s'intéressa aussi à la régulation et à la différenciation embryonnaires et fut un des premiers à évoquer les possibilités de clonage humain.
A la fin des années 20 il remplaça le noyau d'un embryon de salamandre par un noyau issu d'un embryon à 16 cellules.
Il évoqua en 1938 la possibilité de greffer le noyau des cellules des premiers stades embryonnaires dans le cytoplasme d'un ovocyte énucléé. Il proposa cette pratique qui, écrivait-il, « semble à première vue quelque peu fantastique ». Il devenait alors un des premiers à évoquer le clonage des animaux et ... de l'Homme.
6) Une fraude embryologique
En 1874 Ernest Haeckel dans l'Histoire de la création des êtres organisés enseignait que la phylogénèse se retrouvait dans l'ontogénèse. Cela voulait dire que lors de son développement, l'embryon passait par les stades qui avaient été ceux de ses ancêtres (poissons, ...). Pour bien montrer que tous les embryons se ressemblent à un stade précoce, appelé phylotypique, il présentait des planches comparatives d'embryons de différentes espèces:
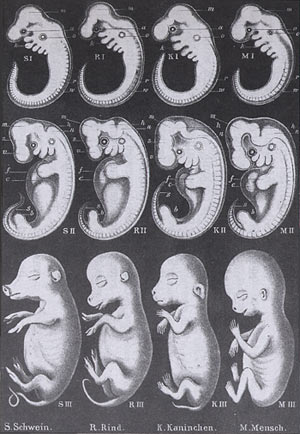
oder Anthropogenie, oder Entwichlungsgeschichte des Menschen
Ernest Haeckel 1874
Aussi célèbre que Darwin à son époque, Haeckel pensait que les animaux évoluaient quand apparaissaient de nouveaux stades embryonnaires, s'ajoutant ainsi aux stades précédents.
Mais pour mieux imposer sa théorie et ce stade phylotypique, il a falsifié les dessins de la première ligne...
Mickaël Richardson a comparé différents embryons d'animaux et a constaté que les embryons au même stade de développement n'ont pas la même taille et que leurs formes sont très différentes. Les dessins d'Haeckel contiennent de nombreuses erreurs.
Haeckel a reconnu lui-même dans différents journaux: "Un petit nombre (six à huit pour cent) de mes dessins d'embryons sont des faux [...], c'est-à-dire ceux pour lesquels le matériel disponible est si incomplet et si insuffisant que j'ai été contraint de compléter et de reconstruire les chaînons manquants..."
Mickael Richardson "Une fraude en embryologie" Mai 1998 numéro 247 Pour la Science p10-12
5) Sites web
- La naissance de la biologie moléculaire
- De nombreux sites web anglo-saxons présentent la controverse Création / Evolution. Il existe une polémique violente aux USA sur ce sujet et les sites web sont très nombreux à avancer leurs arguments.
Pour les créationnistes, l'Homme a été créé par Dieu, et tout ce que dit Darwin est faux. Ils réfutent les arguments évoquant les éléments faisant de l'embryon humain l'aboutissement d'une Evolution, avec l'apparition transitoire d'une queue, d'ouies et d'un sac vitellin. Ils se servent des écrits de Darwin lui-même qui disait que l'évolution de l'oeil était difficile à admettre dans le cadre de sa théorie. Ils insistent bien sûr sur la fraude de Haeckel.
Pour les évolutionnistes au contraire, on retrouve des éléments de l'Evolution (la phylogénèse) dans la création de chaque individu (l'ontogénèse). Les sites sur Darwin fleurissent. Ils essayent de diffuser l'information au sein des écoles. On retrouve aussi des contacts avec les universités comme The Institute of Human Origins.

The Talk.Origins Archive donne accès aux forums Usenet sur l'Evolutionnisme et le Créationnisme. La page des liens est très bien faite. Ce site se veut impartial dans la présentation du débat.
6) Bibliographie
Balinsky, B.I. An Introduction to Embryology (SCP, 1981).
Herbst, C. 1901. Formative Reize in der tierischen Ontogenese. Ein Beitrag zum VerstSndnis der tierischen Embryonalentwicklung. Georgi, Leipzig.
Geinitz, B. 1925. Embryonale Transplantation zwischen Urodelen und Anuren. Roux' Arch. f. Entw. mech. 106: 357 - 408.
Horder, T.J. and others. A History of Embryology (Cambridge Univ. Press, 1986).
King, H. D. 1905. Experimental studies on the eye of the frog embryo. Arch. Ent. Mech. 19: 85 - 107.
Mann Ida The development of the human eye. Cambridge Univercity Press, 1928
Mann Ida Developmental abnormalities of the eye. Cambridge Univercity Press, 1937
Mann Ida The Science of Seeing (with Antoinette Pirie). Pelican Book 1946
Mann Ida The cokney and the crocodile (as Caroline Gye) Faber & Faber 1962
Mann Ida China 13 (as Caroline Gye) Faber & Faber 1964
Mann Ida Race, Climate and Eye Disease Thomas, Springfield 1966
Mann Ida The Chase Fremantle Arts Centre Press 1983
Marx, A. 1925. Experimentelle Untersuchungen zur Frage der Determination der Medullarplatte. Roux' Arch. f. Entw. mech. 105: 20 - 44.
Mayr, E. (1982) Histoire de la biologie (trad française : Fayard, 1989
Morgan, T.H., Sturtevant, A.H., Muller, H.J. & Bridges, C. The mechanism of mendelian heredity. New-York, 1915.
Spemann, H. 1901. Ýber Correlationen in der Entwicklung des Auges. Verhand. Anat. Ges. 15: 61 - 79.
Saha, M. 1991. Spemann seen through a lens. In Gilbert, S. F. (ed.) 1991. A Conceptual History of Modern Embryology. Plenum Press, NY. p. 91 - 108.
Sander, K. 1993. Hans Spemann, Hilde Mangold und der "Organisatoreffekt" in der Embryonalentwicklung. Akademie-Jour. (Jan. 1993): 7-10.
Spemann, H. 1907a. Neue Tatsachen zum Linsenproblemen. Zool. Anz. 31: 379 - 386.
Spemann, H. 1907b. Zum Problem der Correlation in der tierischen Entwicklung. Verhadl. deutsche zool. Gesell. 17: 22 - 49.
Watson, J.D. & Crick, F.H.C. 1953 A structure for desoxyribose nucleic acid. Nature 171, 737-738.
Génétique pour tous
|
|
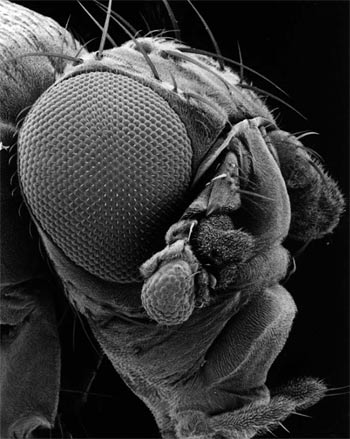
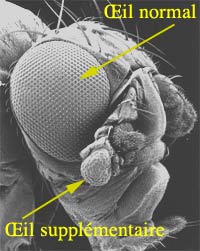
Des yeux à la place des antennes
Mouche drosophile transgénique
Avec l'aimable autorisation du Pr. Gehring |
1) L'Evolution
Darwin lui-même dans "L'origine des espèces" considérait que l'évolution de l'oeil était difficile à admettre dans le cadre de sa théorie de sélection des espèces :
"Il semble absurde au possible, je le reconnais, de supposer que la sélection naturelle ait pu former l'oeil avec toutes les inimitables dispositions qui permettent d'ajuster le foyer à diverses distances, d'admettre une quantité variable de lumière et de corriger les aberrations sphériques et chromatiques."
ou en anglais:
"To suppose that the eye, with all its inimitable contrivances for adjusting the focus to different distances, for admitting different amounts of light, and for the correction of spherical and chromatic aberration, could have been formed by natural selection, seems, I freely confess, absurd in the highest possible degree".
Quelle différence, en effet, entre un oeil de mouche qui comprend 800 unités élémentaires (des ommatidies), chacune contenant 8 neurones photorécepteurs, et un oeil humain qui comprend des millions de cellules.
On se rend compte que malgré l'évolution des espèces animales certains caractères génétiques ont été conservés. Ainsi, certains gènes de régulation servent à spécifier le positionnement des cellules le long de l'axe crânio-caudal (de l'avant vers l'arrière). Ces gènes sont retrouvés chez les vertébrés et les invertébrés, et ont traversé 600 millions d'années.
On assiste également à une stabilité des gènes nécessaires pour la formation de l'oeil. Le gène humain PAX6 est un de ceux la. Les 422 acides aminés de la protéine synthétisée chez l'Homme grâce au gène PAX6, sont identiques chez la souris, et sont quasiment identiques (97%) chez les poissons. On le retrouve aussi chez un ver plat (Dugesia trigrina), un ver némerte (Lineus sanguineus), un calmar (Loligo vulgaris), une ascidie (Phallusia mammilata) et les insectes.
Ce gène régulateur 'maître' PAX6 va entraîner une cascade d'événements issus de 2000 à 3000 gènes qui vont finalement aboutir à la formation de l'oeil.
PAX6 s'exprime aussi pour la formation du tube nerveux dorsal chez les vertébrés et dans la chaîne nerveuse ventrale chez les invertébrés. Ceci semble confirmer que pour comparer le plan d'élaboration d'un invertébré avec un vertébré, il faut seulement le retourner sens dessus dessous.
Geoffroy Saint-Hilaire, formula déjà en 1796 cette idée: "C'est qu'il semble que la nature s'est enfermée dans certaines limites et n'a formé tous les êtres vivants que sur un plan unique, essentiellement le même dans son principe, mais qu'elle a varié de mille manières dans toutes ses parties accessoires". Il pensait que tous les animaux sont constitués selon une même organisation, suivant l'axe antéro-postérieur et dorso-ventral. Pour le démontrer, il retournait un homard, plaçant ainsi le système nerveux en position haute, comme chez les vertébrés.
Georges Cuvier s'opposa violemment à cette idée, en tant que créationniste il croyait au contraire en la séparation des règnes animaux. Bien que seul Cuvier soit resté dans la mémoire collective, il faut considérer Geoffroy Saint-Hilaire comme le père des gènes du développement.
2) Gènes homéotiques
Les gènes sont des fragments d'ADN et vont jouer un rôle prédominant dans l'élaboration de l'organisme durant l'embryogénèse.
On appelle homéotiques les gènes qui permettent aux organes d'être formés à la bonne place.
Les mutations homéotiques atteignent les gènes homéotiques et transforment le segment n+1 en segment n. Lewis a ainsi décrit la mutation Bithorax, transformant une partie du troisième segment thoracique T3 normalement porteur de balanciers, en segment T2 porteur d'ailes (cliché de gauche). Au lieu d'avoir une mouche drosophile à 2 ailes, ce qui est normal, on a pu obtenir une mouche à 4 ailes. Le segment n+1 thoracique correspondant aux balanciers (petits éléments sur le côté du corps), a été remplacé par le segment n (les ailes). On a ainsi créé une mouche avec 4 ailes.
Les mutations de ce type permettent parfois le remplacement d'un organe par un autre. Ainsi la mutation homéotique Antennapedia transforme les antennes de la drosophile en pattes, comme on peut le voir sur le cliché de droite ci-dessous.
|

Drosophile bithorax
Une paire d'ailes supplémentaire
est apparue à la place des balanciers
|
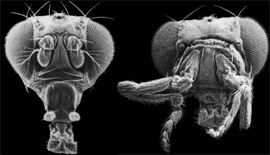
Drosophile normale et antennapedia
A droite des pattes remplacent les antennes
Cliché Dr. Rudi Turner
|

Splendide cliché d'une drosophila melanogaster antennapedia
Cliché dû à l'obligeance du Pr David Cribbs
3) Des yeux rouges sur les pattes
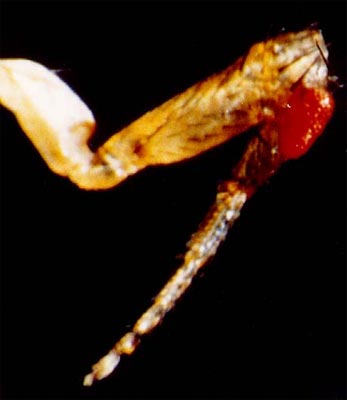
Oeil surnuméraire sur une patte de mouche
Avec l'aimable autorisation du Pr. Gehring
On décrit des mutations appelées "small eye" (Sey) chez la souris, et "Aniridia" chez l'Homme, qui causent des anomalies comparables (petits yeux et absence d'iris). Les deux séquences des protéines sont identiques. Il faut que la souris soit hétérozygote pour que l'on se rende compte de cette anomalie phénotypique. Les sourishomozygotes meurent à l'état embryonnaire, sans yeux et avec un système nerveux anormal.
Les mutations small eye et Aniridia affectent donc le même gène, identique de la souris à l'Homme, ce sont des gènes orthologues (même gène dans des espèces différentes)

Oeil ectopique d'une drosophile transgénique
Cliché dû à l'obligeance du Pr David Cribbs
Le gène qui dirige la formation de l'oeil est le gène PAX6.
Le gène équivalent chez la mouche drosophila melanogaster, est appelé gène eyeless. Il initie la création de l'oeil dans son ensemble et a été séquencé, avec l'aide du hasard, par Rebecca Quiring qui cherchait à séquencer un autre gène.
On a pu 'créer' des mouches avec 14 yeux, dans le but d'étudier le développement des organismes. Walter J.Gehring, en 1995, a activé la transcription de eyeless dans différentes parties du corps des larves de drosophiles et a pu constater la présence d'yeux sur les pattes , les antennes et les ailes. eyeless était donc bien le gène source dirigeant la création de l'oeil chez la mouche. Ces yeux étaient normaux et les cellules visuelles fonctionnaient, mais les yeux n'étaient pas connectés au cerveau.
L'équipe de recherche transféra le gène Pax6 de la souris dans une larve de mouche et vit également apparaître des yeux surnuméraires de mouches sur les ailes et les pattes. La mouche sait donc lire le gène de la souris ! Le gène de la souris sert de commutateur et entraîne le fonctionnement des gènes de la mouche, ce qui explique que ce soit bien un oeil de mouche qui soit formé.
Pourtant ces deux espèces ont divergé, il y a 500 millions d'années.
Par simplification PAX6 correspond à 'small eye' chez la souris, 'eyeless' chez la mouche et 'aniridia' chez l'Homme. Tous ces gènes sont orthologues.

Yeux rouges ectopiques d'une drosophila melanogaster
Cliché dû à l'obligeance du Pr David Cribbs
Des expérimentations ultérieures ont permis de créer des grenouilles (Xenopus) avec trois yeux. Le troisième oeil apparut à l'arrière de la tête, était plus petit que les yeux habituels mais possédait tous les éléments (cristallin, rétine...).
Nous vous proposons un intéressant texte public en anglais de l'équipe du Pr Gehring : Eyeless initiates the expression of both sine oculis and eyes absent during Drosophila compound eye development
ainsi qu'un autre de Veraska, Del Campo et McGinnis, en anglais : Developmental Patterning Genes and Their conserved functions, From model organisms to Humans.
Ainsi, on peut dire que l'embryologie de l'oeil de l'Homme, de la mouche et de la souris est pilotée par le même gène bien que les yeux de ces trois espèces soient tout à fait différents !! Cela veut sans doute dire que ce gène (PAX6 ou small eye ou eyeless) est très ancien et commun à de nombreuses espèces. L'évolution a fait diverger les espèces au fil des millions d'années mais elles ont gardé un souvenir commun, le gène qui dirige la formation de l'oeil.
Pour expliquer les différences entre les différents yeux des espèces, on pense qu'après le gène commun se trouvent des gènes intermédiaires responsables de la construction de l'oeil.
Des mutations de ces gènes vont entraîner différentes anomalies oculaires, telle qu'une Aniridie.
L'aniridie correspond à l'absence d'iris des deux côtés. A l'examen on se rend compte qu'on voit l'ensemble du cristallin, et qu'il n'existe qu'une mince collerette d'iris. Elle peut s'accompagner de complications ophtalmologiques, comme un glaucome, une hypoplasie maculaire, une luxation du cristallin, des opacités cristalliniennes ou uneamétropie. Il est important de rechercher un syndrome général lorsque l'aniridie s'associe à une délétion chromosomique en 11p13. En effet on peut déceler unnéphroblastome (tumeur de Wilms) ou un gonadoblastome, dans le cadre d'un syndrome WAGR (Wilms tumor, Aniridia, Genito-urinary malformation, mentalRetardation).
Différentes mutations génétiques sont responsables d'autres dysgénésies du segment antérieur associant des anomalies de la cornée, de l'iris et de l'angle irido cornéen avec glaucome (syndrome de Peters, de Rieger ou d'Axenfeld).
...quasiment identiques, dans le règne animal, comme le gène RPE65. On retrouve une structure comparable à plus de 95% chez la souris et chez l'Homme. Ce gène peut être déficient comme dans l'amaurose congénitale de Leber. Il code une protéine RPE65 qui joue un rôle important, bien que mal connu, dans la synthèse de la rhodopsine.
Ana Boulanger, Suyan Liu, Shirley Yu, T. Michael Redmond Sequence and structure of the mouse gene for RPE65 Mol Vis 2001; 7:[pagination pending]
5) Archéophotochimie de la vision
On a pu être étonné de la conservation de PAX6 au fil de l'Evolution, mais on s'est rendu compte que la Nature avait choisi des voies différentes pour les réactions photochimiques induites dans la rétine par la lumière.
L'élément clef dans le phénomène de la vision, c'est le rôle de la lumière dans les réactions photochimiques qui se produisent au niveau de la rétine, et qui vont donner un influx nerveux vers le cerveau.
La réaction chimique capitale est la photoisomérisation du rétinaldéhyde. Cette réaction semble avoir été conservée au fil des espèces animales
Chez les procaryotes, c'est l'action d'une pompe à protons (bactériorhodopsine) fonctionnant sous l'influence de la lumière qui va créer de l'ATP (adénosine triphosphate). Chez les eucaryotes ce mécanisme est utilisé pour la photoréception.
L'association du rétinaldéhyde et d'une protéine nommée opsine forme la rhodopsine. L'opsine fait partie d'une classe de récepteurs transmembranaires couplées auxprotéines G. Chez les métazoaires, les opsines sont une sous-famille distincte qui a dû évoluer à partir d'un ancêtre commun.
La rhodopsine est la molécule capitale qui permet la vision. Un seul photon de lumière suffit à activer une molécule de rhodopsine, en isomérisant le pigment visuel, le 11-cis-rétinal en tout-trans-rétinal, ce qui induit un changement de conformation de la molécule de rhodopsine aboutissant à la métarhodopsine II (forme activée).
Bien qu'on ait un processus comparable de photoisomérisation à partir du 11-cis-rétinal (vertébrés) ou de déhydro-ou d'hydroxy-11-cis-rétinal (invertébrés), les réactions chimiques qui suivent ne sont pas les mêmes.
Chez les vertébrés, l'activation de la rhodopsine par la lumière entraîne, par l'intermédiaire de protéines G spécifiques, la modification du taux de GMP cyclique. Ce GMP cyclique commande un canal sodium. Dans le noir les niveaux de GMP cyclique sont hauts et le canal est ouvert, la membrane est dépolarisée et la synapse active, larguant des neurotransmetteurs A la lumière, l'activation de la rhodopsine entraîne l'activation d'une enzyme phosphodiestérase qui va hydrolyser le GMP cyclique. Donc cette molécule devient rare, ce qui va fermer le canal sodium, ce qui stoppe l'émission du neurotransmetteur. Cette information est relayée par un jeu complexe de cellules bipolaires et de cellules horizontales.
Chez les invertébrés,
Le processus de transduction visuelle est différent. La lumière va activer la rhodopsine, qui, par une protéine G différente va activer une enzyme phospholipase C. Cela va donner la production de deux messagers, le diacylglycérol et l'inositol triphosphate. Ces deux molécules vont entraîner deux voies différentes : le premier active une protéine kinase C, le second active un canal calcium.
Au total
L'action de la lumière sur le pigment visuel est commune aux vertébrés et aux invertébrés mais le processus de transduction visuelle est différent. Il y a encore desinconnues sur le fonctionnement des photorécepteurs, notamment sur l'adaptation des photorécepteurs à la lumière, sur la régulation de la transmission synaptique, sur les processus d'élaboration des organelles contenant le pigment visuel, et sur le cas particulier des cônes, moins bien connus que les bâtonnets.
6) Prix Nobel
Le Prix Nobel fut attribué en 1995 à Edward B. Lewis, Christianne Nüsslein-Volhard et Eric F. Wieschaus pour avoir exploré le contrôle génétique du développement embryonnaire.
|

Edward B. Lewis
|

Christianne Nüsslein-Volhard
|

Eric F. Wieschaus
|
Ils mirent en évidence les gap-genes qui sont sollicités très tôt dans l'embryon et permettent de donner le plan d'ensemble avec un axe crânio-caudal. Puis les pair rule-genes vont entraîner la segmentation de l'embryon. Enfin les segments polarity-genes donnent leur spécificité à la tête et au secteur caudal.
Il trouva une colinéarité dans le temps et dans l'espace entre l'ordre des gènes dans le complexe bithorax et leurs régions cibles.
Lewis déclara que ce prix était "une reconnaissance du pouvoir de la génétique pure".
7) La drosophile aux yeux rouges
Nous vous conseillons le livre "La drosophile aux yeux rouges" qui décrit la génétique actuelle et les progrès de ces dernières années. Cette quête est très loin du but qui permettrait de comprendre l'ensemble de la formation de l'organisme. Nous ne sommes qu'au début d'une longue et passionnante exploration de nos gènes.
|

|

Pr. Walter.J. Gehring
"Quoi de plus stupéfiant que le développement d'une embryon ? Comment les cellules savent-elles qu'elles doivent placer les yeux sur la face et non sur la cuisse de l'individu qu'elles forment ? Pourquoi l'oublient-elles parfois pour donner connaissance à un monstre ?
Walter Gehring retrace les progrès récents de la génétique du développement embryonnaire dont il est l'un des plus éminents spécialistes. Il raconte la traque planétaire des gènes qui contrôlent l'exécution du plan universel que suit la formation des organismes supérieurs, de la mouche à l'homme. Il décrit en même temps la concurrence impitoyable que se livrent les scientifiques, dont la vertu cardinale devient l'opportunisme clairvoyant.
Où l'on commence à comprendre comment nous sommes fabriqués..."
Editions Odile Jacob Sciences ISBN 2.7381.0696.X
|
|

|
Pour ceux qui seraient pris du virus de la Connaissance, il est toujours bon de redécouvrir le livre de Darwin, "L'origine des espèces" (1859).
Le chapitre VI est très intéressant car il évoque les "Difficultés de la Théorie" avec, en particulier, les "Organes de perfection extrême" dont l'oeil est le principal représentant.
Editions GF-Flammarion ISBN 2-08-070685-3
|
Génétique spé
Les notions générales sont regroupées sur la page Génétique.

1) PAX6 et les gènes homéotiques
Comme on l'a vu dans la page de génétique générale, c'est le gène PAX6 qui dirige la formation de l'oeil chez de nombreuses espèces animales et chez l'Homme.
On a retrouvé en 1983 une même chaîne de 180 paires de bases dans ces gènes homéotiques, appelée Homeobox ou Homéoboite.
Les mammifères possèdent quatre groupes de gènes homéotiques. On les appelle des complexes Hox (pour Homeobox) et ils sont chacun sur un chromosome différent. Les quatre complexes Hox proviennent de la duplication des chromosomes. On pense qu'il existait autrefois un complexe ancestral et, qu'au cours de l'évolution, il s'est produit une duplication de ce complexe. L'ordre de ces complexes Hox sur chacun des quatre chromosomes est tout à fait similaire, on dit qu'ils sont paralogues (par exemple HoxA3, HoxB3, HoxC3, HoxD3).
Les gènes qui donnent les mutations oculaires contiennent à la fois une homeobox et une "paired box" codant pour une deuxième région de la protéine, également capable de se fixer sur l'ADN des gènes cibles. Les gènes de régulation contenant une paired box constituent la famille des gènes pax (pour paired box) par analogie avec la famille des gènes Hox contenant une homeobox.
Les gènes pax illustrent ce que François Jacob a appelé "le bricolage de l'évolution" car ils sont constitués de différents morceaux. Certains gènes pax n'ont qu'une paired box (ou boite paired), d'autres ont une paired box et une homeobox (homéoboite), d'autres encore ont un paired box et une homeobox partielle, codant le bras N-terminal et la première hélice alpha seulement.

Expression du gène Pax6 dans la rétine de caille
Embryon de 8 joursLes noyaux cellulaires apparaissent en bleu. La présence de l'ARN du gène Pax6 visualisé par les grains d'argent de l'hybridation moléculaire apparaît en jaune.
a : Epithélium pigmenté
b : couche (bleue) des photorécepteurs n'exprimant pas Pax6
c : couche (jaune) des cellules horizontales exprimant Pax6
d : cellules amacrines
e : neurones ganglionnaires exprimant Pax6
La couche sombre entre d et e correspond à la couche plexiforme interne, acellulaire.
2) Homéoprotéines et homéodomaine
Les gènes homéotiques déterminent la synthèse de protéines régulatrices qui activent ou bloquent l'activité d'autres gènes cibles en se fixant directement sur l'ADN.
Ces protéines régulatrices sont appelées homéoprotéines et elles possèdent une séquence d'acides aminés commune à toutes: c'est l'homéodomaine.
L'homéodomaine est une chaîne particulière d'acides aminés, qui reconnaît une séquence précise d'ADN sur laquelle elle se fixe. Les premiers gènes trouvés encodant des protéines avec homéodomaines furent ceux qui contrôlent chez la drosophile les gènes de développement.
L'homéodomaine a une longueur de 60 acides aminés et a une structure en trois dimensions, en trois hélices alpha. Cela donne un motif HTH (hélice-tour-hélice) qui va se positionner entre les brins de la molécule d'ADN pour que la transcription puisse se faire. Le domaine HTH est le plus vieux motif de liaison à l'ADN car on le trouve dans une protéine répresseur du phage lambda, ce qui veut dire qu'il préexistait chez les procaryotes. La séquence de paires de bases minimum reconnue par l'homéodomaine est la séquence TAAT.
Le motif HTH est présent chez l'ancêtre des procaryotes et l'ancêtre des eucaryotes (il n'est en effet pas sûr du tout que les eucaryotes dérivent des procaryotes).
3) Paired Box
Une paired box code pour le domaine paired qui comme l'homéodomaine est un motif de liaison à l'ADN.
Le sigle paired vient de ce que ce type de séquence a été initialement identifié dans le gène paired de la drosophile, ce gène codant pour une protéine (la protéine paired) impliquée dans le développement précoce de l'embryon. La structure du domaine paired déduite par l'analyse cristallographique est très proche de celle del'homéodomaine avec trois hélices alpha, la troisième placée dans le plan perpendiculaire aux deux autres s'intercalant dans le grand sillon de l'ADN. La particularité dePAX6 c'est que son domaine paired code en fait deux motifs de liaison à l'ADN. La portion NH2 et la portion C-terminale peuvent se lier à l'ADN indépendamment l'une de l'autre et sur des séquences différentes, mais toutes deux ressemblent fort en structure à l'homéodomaine (3 hélices alpha chacune avons-nous dit).
Les séquences reconnues dans l'ADN sont toutefois différentes pour les domaines paired et homeo. Il y a 9 gènes pax chez les vertébrés, pax1 et pax9 étant les seuls à ne pas s'exprimer dans le système nerveux.
Dans l'oeil PAX6 s'exprime dans la placode cristalline puis dans le cristallin, dans la neurorétine (cellules ganglionnaires, amacrines et horizontales) la rétine pigmentaire.
Plus de précisions avec:
Growth and specification of the eye are controlled independently by Eyegone and Eyeless in Drosophila melanogaster Maria Dominguez, Dolors Ferres-Marco, Francisco J Gutierrez-Avinô, Stephan A Speicher & Monica Beneyto Nature Genetics January 2004
Two Pax are better than one Richard S Mann Nature Genetics January 2004
et en français:
Le domaine paired: divers moyens de construire une protéine PAX m/s vol 15 avril 99
4) D'autres gènes rentrent en jeu
Pax2 s'exprime au début du développement exclusivement dans la partie ventrale de la vésicule optique puis reste restreint aux cellules de la racine du nerfs optique (ouPax6 ne s'exprime pas).
L'invalidation de Pax2 chez la souris conduit a des colobomes par défaut de fermeture de la fissure choroidienne qui est envahie par les cellules de la rétine pigmentaire.Pax2 s'exprime également dans le rein ou son absence induit également des défauts de développement. Les cellules qui expriment Pax2 n'expriment pas Pax6 et réciproquement.
Il a été récemment montré que ces deux gènes inhibaient mutuellement leur expression. Pax6 s'exprime dans le pancréas endocrine et son expression est indispensable pour la formation des îlots a (glucagon). Pour qu'il y ait un effet sur le pancréas, cela nécessite une mutation sur les deux allèles (un seul allèle touché, pancréas normal) par contre, un seul allèle touché, les yeux sont anormaux (une mutation sur les deux allèles est de toute façon létale tout de suite après la naissance à cause de troubles majeurs dans le fonctionnement du cerveau). Il n'y a pas d'autre gène pax à s'exprimer dans l'oeil (mais il y a pléthore de gènes à homéodomaine dont aucun n'a un effet aussi fort sur le développement de l'oeil que Pax6).
- Le gène CRX (Cone Rod homeoboX)
Ce gène est fondamental dans le développement, la différenciation et la maintenance des photorécepteurs rétiniens, cônes et bâtonnets. Il code un facteur de transcription mal connu pour l'instant. Voir OMIM
Il semble que des pathologies comme la cone-rod dystrophy-2, certaines rétinites pigmentaires et l'amaurose congénitale de Leber puissent être dues à des mutations de ce gène capital.
Germot Agnès, Spengler Tatjana, Harrison Gavan and Mazan Sylvie Structural evolution in mammals of Crx, an orthodenticle homeobox gene involved in retinal diseases in humans. Equipe ATIPE UPRES A CNRS 8080 "Développement et Evolution" Bâtiment 441 Université Paris 11 91405 Orsay cedex France.
Mazan Sylvie, Equipe ATIPE de l'UPRES-A 8080 Diversification fonctionnelle des gènes de la classe orthodenticle chez les crâniates
"...Trois autres gènes, que nous avons identifiés respectivement chez la roussette, chez un polyptère (le poisson-roseau Erpetoichthys calabaricus), et récemment, chez le xénope, définissent en outre une troisième classe d'orthologie (Otx5). Nos analyses phylogénétiques suggèrent fortement que le gène humain Crx, impliqué dans desdégénérescences rétiniennes héréditaires chez l'homme, est un membre très divergent de cette troisième classe."
Une famille de gènes donne le phénotype "sine oculis" (sans yeux) chez la drosophile. On retrouve cette famille chez la souris et elle contient au moins six membres, dont l'un d'eux appelé Six3 correspond au gène "sine oculis". Il joue un rôle dans la formation du nerf optique, des vésicules optiques, des cristallins et des placodes nasales. Son rôle mal connu semble donc très important.
Ce gène joue un rôle dans la différenciation de la neuro-rétine. La mutation du gène de la souris donne l'anomalie "ocular retardation". Chez ce mutant, la couche des cellules bipolaires manque complètement et l'oeil est plus petit. Ce gène contient une homeobox mais pas de paired box. Il s'exprime surtout dans la zone qui va donner la rétine et, chez l'homme, il s'exprime seulement dans les cellules bipolaires.
Ce gène pourrait correspondre à des anomalies de l'oeil (microphtalmies).
- Le gène PITX2 (anciennement RIEG)
Chez l'homme, la mutation de ce gène est responsable du syndrome de Rieger (1935) qui associe des anomalies de la chambre antérieure de l'oeil avec glaucome, une hypoplasie dentaire, un dysmorphisme crânio-facial et une anomalie de la paroi ombilicale. On décrit six mutations de ce gène.
La maladie est autosomale dominante.
On a décrit ce gène en 4q25 et un autre locus fut trouvé en 13q14.
- Le gène MITF (Microphthalmia-associated transcription factor)
Les vésicules optiques comprennent deux feuillets, l'un qui est externe et qui va donner l'épithélium pigmenté de la rétine et l'autre qui est plus interne et qui va donner larétine neuro-sensorielle avec les cellules visuelles, cônes et bâtonnets. Les deux feuillets vont se différencier grâce à des molécules extérieures, des FGF (fibroblast growth factor) qui proviennent de la surface ectodermique. Ils vont orienter la rétine proche en neurorétine.
Des expérimentations ont permis de placer ces facteurs dans la partie postérieure de la vésicule optique et l'on a assisté à un différenciation neuro-sensorielle du feuillet rétinien qui devait devenir épithélium pigmenté. Inversement, l'ablation de l'ectoderme proche des vésicules optiques a empêché la différenciation du feuillet sensoriel qui est devenu pigmenté.
La mutation de ce gène chez la souris est appelée 'microphthalmia' (mi) et donne une microphtalmie et un défaut de pigmentation de l'oeil et de la peau. Ces mutations chez l'Homme donnent le syndrome de Waardenburg de type II et ont été décrites en 3p14.1-p12.3 (voir OMIM).
- Le gène BMP7 (Bone morphogenetic proteins)
Si ce gène est muté, on se rend compte que le gène PAX2 ne fonctionnera pas, comme s'il avait besoin de facteurs d'induction issus de BMP7. Les souris mutantes homozygotes ont une anophtalmie dans 60% des cas et une microphtalmie dans 40% des cas. On note un défaut de transformation de la placode cristallinienne en vésicule cristallinienne. L'ARNm BMP7 est retrouvé dans la vésicule optique et la placode ectodermique.
Ces protéines BMP appartiennent à la grande famille des TGFbêta (transforming growth factor bêta)
Ce gène est important car il entraîne la formation de facteurs diffusibles nécessaires pour la formation de l'oeil. Les gènes hedgehog ont été retrouvés chez la drosophile, le poulet, la grenouille et l'homme. Les protéines produites grâce au gène hedgehog et au gène decapentaplegic (dpp) sont impliquées dans la différenciation des photorécepteurs de la drosophile.
Chez la drosophile on a décrit deux gènes intermédiaires qui sont 'twin of eyeless' nommé Toy, et drosocrystallin. Chez cet animal en effet on a trouvé un homologue dePax6 nommé toy. Il provient d'une duplication qui intervient tardivement dans l'évolution de l'insecte mais il s'exprime plus tôt que Pax6 dans l'embryogénèse. Toy est nécessaire pour l'initialisation de eyeless et dirige la formation de l'oeil grâce à eyeless.
Eyeless et Toy activent un ensemble de gènes de transcription : sine oculis (So), eye absent (eya) et dachshund (dac). Trois gènes homologues de Eya ont été retrouvés chez la souris.
Chez l'homme, un analogue de Eya a été repéré et est primordial pour le développement de l'oeil et du rein. Ce gène humain EYA1 altéré va donner un BOR (branchio-oto-renal) syndrome, une cataracte et des anomalies du segment antérieur.
Le deuxième gène intermédiaire encode pour une protéine appelée drosocrystalline; cette protéine initialement cuticulaire est utilisée en tant que protéine du cristallin.
- Le récent article de Justin P. Kumar et Kevin Moses EGF Receptor and Notch Signaling Act Upstream of Eyeless/Pax6 to Control Eye Specification. Cell, Vol. 104, 687-697, March 9, 2001 Cell Press. met l'accent sur les sept facteurs qui commandent l'élaboration de l'oeil de la drosophile ; twin of eyeless (toy), eyeless (ey), eyes absent (eya), sine oculis(so), dachshund (dac), eye gone (eyg), et optix (opt). Les auteurs considèrent que tous ces facteurs génétiques ne font pas simplement partie d'une hiérarchie, mais participent plutôt à un réseau d'élaboration de l'oeil avec de nombreuses interactions. La formation d'oeil ectopique ne peut se faire que dans les régions du corps qui expriment les gènes hedgehog (hh) et decapentaplegic (dpp). Les auteurs ont déterminé que les facteurs Notch and Egfr sont des gènes précurseurs, agissant en amont de Pax6 et "are the Shiva and Brahma of developmental control".
5) Prospective
Les travaux sur la génétique ont permis de mieux comprendre la différenciation cellulaire. Comment une cellule embryonnaire va-t-elle donner un globule rouge ou bien une cellule rétinienne ?
Il est permis d'imaginer qu'on pourra un jour influencer la différenciation cellulaire et l'orienter dans une voie choisie à l'avance. On arrive actuellement à dédifférencierune cellule pigmentée de rétine de caille et à lui faire, en quelque sorte, remonter le cours du temps pour lui redonner une jeunesse et une nouvelle destinée, par exemple la transformer en cellule du neuro-épithélium. On est même arrivé à transformer une cellule de la rétine pigmentée en neurone, ce qui est tout à fait intéressant.
On a cru longtemps que la différenciation d'une cellule était une voie sans issue. On se rend compte qu'au contraire, il est possible de modifier l'expression de son génome pour qu'elle se transforme en une autre cellule. Cela laisse la porte ouverte à de nombreuses possibilités. Ainsi on peut imaginer qu'on reconstituera des neurones dans lesmaladies neuro-dégénératives, ou bien des cellules visuelles et/ou pigmentées dans les nombreuses dégénérescences rétiniennes sans traitement à l'heure actuelle.
La récente publication de Andy J. Fischer et Thomas A. Reh dans Nature Neuroscience (2001) 4: 247-252, "Muller Glia are a potential source of neural regeneration in the postnatal chicken retina" décrit une expérimentation très intéressante. Après lésion de la rétine de poulet grâce à une injection intra-vitréenne de NMDA (N-methyl-D-aspartate), les scientifiques ont assisté à une dédifférenciation des cellules de Muller (la seule cellule gliale dérivée de la cupule optique). Celles-ci ont proliféré et certaines ont perdu leur caractère phénotypique glial pour exprimer des facteurs de transcription embryonnaires, comme Pax6, chx10 et CASH1. Certaines des cellules de Muller setransdifférencient en neurones et expriment un antigène neurofilament-like.
Cela met en évidence les possibilités du tissu glial à se dédifférencier et à trouver des capacités de transdifférenciation, même partielles.
Le Professeur Spyros Artavanis-Tsakonas, dans sa leçon inaugurale au Collège de France (chaire de biologie et génétique du développement), déclarait le jeudi 26 avril 2001 :"Pouvoir modifier une destinée cellulaire en manipulant un gène spécifique intégré à une voie spécifique pourrait avoir d'importantes conséquences en médecine. De nombreuses maladies dysplasiques, cancers compris, pourraient être soignées de cette manière. Moyennant par exemple, la manipulation d'une cellule maligne pour faire de sa destinée quelque chose de moins pathogène. Si nous parvenons à comprendre les règles qui régissent la manipulation des destinées cellulaires, peut-être pourrons-nous alors forcer certaines cellules à se différencier en cellules semblables à celles qui ont été atteintes ou supprimées par la maladie. Ces cellules serviraient alors à repeupler les organes atteints, entraînant ainsi la guérison, ou la réduction de l'état pathologique."
Une piste possible de recherche se présente selon Masatoshi Haruta, car il est possible de prélever des cellules de l'iris pour les cultiver et les inciter à se transformer en une couche monocellulaire productrice du pigment visuel, la rhodopsine. On pourrait ainsi peut-être un jour régénérer une rétine malade à partir d'un prélèvement d'iris simple à effectuer par une petite incision cornéenne. Il faut que les cellules iriennes expriment le gène Crx, ce qui n'est réalisable actuellement qu'en injectant ce gène surnuméraire grâce à un vecteur viral. Il dit ceci:
"We show that iris tissue in the adult rat eye, which is embryonically related to the neural retina, can generate cells expressing differentiated neuronal antigens. In addition, the Crx gene transfer induced the specific antigens for rod photoreceptors in the iris-derived cells, which was not seen in the adult hippocampus-derived neural stem cells. Our findings demonstrate a remarkable plasticity of adult iris tissue with potential clinical applications, as autologous iris tissue can be feasibly obtained with peripheral iridectomy."
On a là un exemple expérimental de dédifférenciation-différenciation cellulaire tout à fait passionnante.
Masatoshi Haruta, Mitsuko Kosaka, Yumi Kanegae, Izumu Saito, Tomoyuki Inoue, Ryoichiro Kageyama, Akihiro Nishida, Yoshihito Honda & Masayo Takahashi Induction of photoreceptor-specific phenotypes in adult mammalian iris tissue December 2001 Volume 4 Number 12 pp 1163 - 1164 Published online: 12 November 2001, DOI:10.1038/nn762.
Site web Nature Neuroscience.
6) Cells, embryos and evolution
|
|
Les 650 pages de cet excellent livre américain permettent d'avoir une vue d'ensemble de la biologie moléculaire, de la génétique et del'évolution des espèces animales. Vraiment une référence.
Sommaire :
1) The surprising conservation of cellular processses
2) Contingency
3) Regulatory linkage
4) The exploratory behavior of biological systems
5) Novelty
6) Conditionality and compartmentalization
7) Body plans
8) Axis specification and reproductive strategies
9) Developmental flexibility and robustness
10) Evolutionary diversification of the body plan
11) Evolution and evolvability
|
7) Brève bibliographie
Babinet C., « Une famille de gènes du développement : les gènes pax », Médecine/sciences, 9,87,1993.
Bard, L. A. : Heterogeneity in Waardenburg's syndrome: report of a family with ocular albinism. Arch. Ophthal. 96: 1193-1198, 1978.
Bondurand, N.; Pingault, V.; Goerich, D. E.; Lemort, N.; Sock, E.; Le Caignec, C.; Wegner, M.; Goossens, M. : Interaction among SOX10, PAX3 and MITF, three genes altered in Waardenburg syndrome. Hum. Molec. Genet. 9: 1907-1917, 2000.
Bonini N.M. et K.W. Choi, « Early decisions in Drosophile eye morphogenesis », Curr. Op. Gen. Dev., 5, 507, 1995.
Carroll S.B. , « Homeotic genes and the evolution of arthropods and chordates », Nature, 376, 479, 1995.
Chow RL, Altmann CR, Lang RA, Hemmati-Brivanlou A. Pax6 induces ectopic eyes in a vertebrate. Development 1999 Oct;126(19):4213-22
Gehring W.J. The master control gene for morphogenesis and evolution of the eye, Genes Cells, Vol. 1 (1996) 11-15.
Grindley J.C., D.R. Davidson and R.E. Hill, The role of Pax-6 in eye and nasal development, Development, Vol. 121 (1995) 1433-1442.
Gruss P. et C. Walther, « Pax in development », Cell, 69, 719, 1992.
Halder, G., Callaerts, P. and Gehring, W.J. (1995). Induction of ectopic eyes by targeted expression of the eyeless gene in Drosophila. Science 267, 1788-1792.
Hanson H. et V. Van Heyningen, « pax-6 more than meets the eye », TIG, 11, 268, 1995
Hanson I.M. , J.M. Fletcher, T. Jordan, A. Brown, D. Taylor, R.J. Adams, H.H. Punnett and V. van Heyningen, Mutations at the pax-6 locus are found in heterogeneous anterior segment malformations including Peters' anomaly, Nature Genet., Vol. 6 (1994) 168-173.
Hill R.E., J. Favor, B.L. Hogan, C.C. Ton, G.F. Saunders, I.M. Hanson, J. Prosser, T. Jordan, N.D. Hastie and V. van Heyningen, Mouse small eye results from mutations in a paired-like homeobox-containing gene, Nature, Vol. 354 (1991) 522-525.
Jacob F. , « L'irrésistible ascension des gènes Hox », Médecine/sciences, 10, 145, 1994.
Jordan T. , I. Hanson, D. Zaletayev, S. Hodgson, J. Prosser, A. Seawright, N. Hastie and V. van Heyningen, The human pax-6 gene is mutated in two patients with aniridia, Nature Genet., Vol. 1 (1992) 328-332.
Lawrence P.A. , The making of a fly, Blackwell Scientific Publishing, Oxford, 1992. M W.J. Gehring, « Homeo Boxes in the Study of Development », Science, 236,1245,1987.
Li H.S. , J.M. Yang, R.D. Jacobson, D. Pasko and O. Sundin, Pax-6 is first expressed in a region of ectoderm anterior to the early neural plate: implications for stepwise determination of the lens, Dev. Biol., Vol. 162 (1994) 181-194.
McGinnis W. et R. Krumlauf, « Homeobox genes and axial paterning », Cell, 68, 283, 1992
Moore, K. J. : Insight into the microphthalmia gene. Trends Genet. 11: 442-448, 1995.
Planque N., Turque N., Opdecamp K., Bailly M., Martin P. and Saule S. (1999). Expression of the microphthalmia-associated b-HLH-Zip transcription factor Mi in avian neuroretina cells induces a pigmented phenotype. Cell Growth and Differentiation, 10 : 525-536.
Plaza S., Hennemann H., Moroy T., Saule S. and Dozier C. (1999) Evidence that pou factor Brn-3b regulates expression of Pax-6 in neuroretina cells. Journal of Neurobiology, 41 :349-358.
Quiring R. , U. Walidorf, U. Kloter and W.J. Gehring, Homology of the eyeless gene of Drosophila to the Small eye gene in mice and Aniridia in humans, Science, Vol. 265 (1994) 785-789.
Tomarev S.I. , P. Callaerts, L. Kos, R. Zinovieva, G. Halder, W. Gehring and J. Piatigorsky, Squid Pax-6 and eve development, Proc. Natl. Acad. Sci. USA, Vol. 94 (1997) 2421-2426.
Walther C. and P. Gruss, Pax-6, a murine paired box gene, is expressed in the developing CNS, Development, Vol. 113 (1991) 1435-1449.
Rapport des yeux et du développement de la face
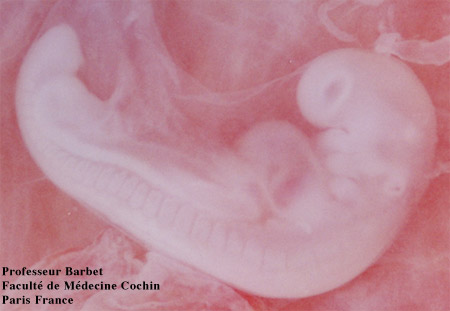
Embryon de 26 jours
A droite, l'extrémité céphalique avec la placode optique (futur oeil)
La tête primitive est formée par la courbure du disque embryonnaire lors de la quatrième semaine. Au début de cette quatrième semaine, la zone "tête et cou" représente environ le tiers de la longueur de l'embryon.
La face se forme progressivement entre la quatrième et la dixième semaine de vie.

Embryon de quatre semainesL'apparition de plusieurs bourrelets de part et d'autre de l'extrémité céphalique de l'embryon va entraîner l'apparition de cinq arcs pharyngiens numérotés I, II, III, IV et V. Cela correspond aux arcs branchiaux des poissons, mais les fentes branchiales ne s'ouvrent jamais chez l'embryon humain. On trouve donc là des éléments communs aux poissons et aux mammifères.

Les 5 paires de fentes branchiales du requin makoLe premier arc pharyngien apparaît le 22ème jour et va donner un bourgeon maxillaire (futur maxillaire) et un bourgeon mandibulaire en dessous (future mâchoire inférieure).
Les autres arcs vont donner différentes structures (étrier de l'oreille, os hyoïde, larynx par exemple).
Progressivement la face se développe à partir de cinq bourgeons, le processus fronto-nasal, les deux processus maxillaires et les deux processus mandibulaires. Chaque processus va converger vers son homologue situé du côté opposé. Ils entourent la membrane bucco-pharyngienne qui va se transformer en stomodeum, la future cavité buccale.
Au cours de la cinquième semaine, on voit apparaître sur le processus fronto-nasal, les placodes nasales.

La face à cinq semaines
Lors de la sixième semaine, elles s'invaginent et une dépression nasale apparaît dans l'ectoderme. Les placodes nasales vont alors être divisées en un processus nasal latéral et médian.. On nomme gouttière naso-lacrymale l'espace situé entre le processus nasal latéral et le bourgeon maxillaire adjacent. L'ectoblaste du plancher de cette gouttière va s'invaginer lors de la septième semaine dans le mésenchyme sous-jacent pour former le conduit lacrymo-nasal qui conduira les larmes des yeux dans le nez. Lorsque ce conduit n'est pas perméable, il est parfois nécessaire que l'ophtalmologiste le débouche avec une sonde, peu après la naissance. C'est le sondage des voies lacrymales.
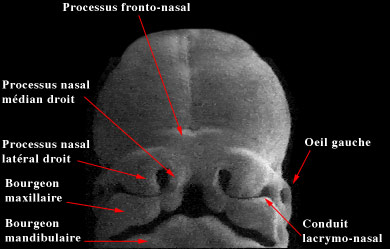
La face au début de six semaines
La face devient très reconnaissable déjà :
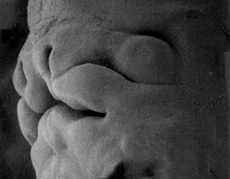
La face humaine à la fin de six semaines
Microscopie à balayage
University of North Carolina
Lors de la septième semaine on assiste petit à petit à la soudure des bourgeons pour former le nez, la mâchoire supérieure et la mandibule. Les yeux qui avaient une position très latérale deviennent plus frontaux.
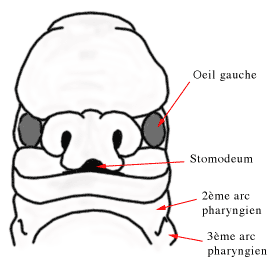
La face à sept semaines
Les anomalies de croissance ou de fusion des bourgeons faciaux vont entraîner des défauts de fermeture, les fentes faciales (fentes labiales, fentes palatines), ou des anomalies plus graves, comme la cyclopie (nous vous épargnons les images).
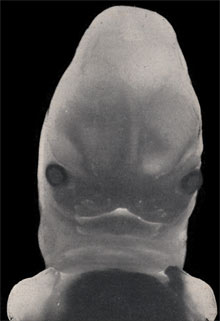
Embryon de sept semaines
Sites web
Bibliographie
Beaumont A. et al., Développement, Dunod, 1994.
Douglas John Ocular Anatomy; The Anatomy, Histology, Embryology, Ontogeny, And Phylogeny Of The Human Eye And Rel Spooner,. London Hatton Press,1957
Earl J. :Wm. D.Zoethou Hazlitt & Walker The embryology anatomy & histology of the eye;the physiology of vision Brown,, Chicago, 1906.
Holden, Warden Andrews An outline of the embryology of the eye, with illus. from original pen-drawings by the author. New YorkG.P. Putnam,1893
Wolpert M L. , Le triomphe de l'embryon, Dunod, 1992.
Vue d'ensemble de l'embryologie de l'oeil

Embryon de 41 jours: une main et un oeil pigmenté
Cliché Pr Barbet Faculté de Médecine Cochin Paris France
Les yeux sont une émanation du cerveau. Il ne s'agit pas d'un organe comme le foie ou le rein, mais d'une expansion du cerveau qui cherche à explorer sonenvironnement. On retrouve cette origine neurologique dans l'embryologie.
Au début de la quatrième semaine, on voit apparaître, de part et d'autre du cerveau, deux dépressions, les gouttières optiques.
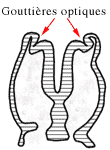
Coupe du cerveau
Embryon de 4 semaines
En s'avançant vers l'ectoderme superficiel, elles vont s'invaginer pour former les vésicules optiques.
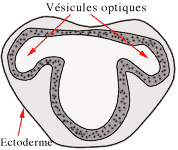
Coupe du cerveau
Embryon de 4 millimètres
Elles vont se transformer en cupules optiques sphériques et creuses, attachées au cerveau par les pédicules optiques (futurs nerfs optiques).
L'ectoblaste à proximité des cupules va s'épaissir pour former les deux placodes optiques (futurs cristallins).
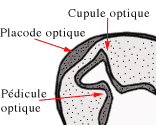
Ces placodes vont s'invaginer pour donner les vésicules cristalliniennes creuses et positionnées dans les cupules optiques.

La vésicule formée va pénétrer dans la cupule optique et se transformer progressivement en cristallin.

A partir de là, on va assister à la fermeture de la fente embryonnaire, ce qui va souder les deux berges des pédicules optiques.
et de façon plus détaillée:
Embryologie descriptive de l'oeil
Trois périodes résument le développement embryologique de l'oeil.
- L'embryogénèse s'étend de la fécondation de l'ovocyte à la fin de la troisième semaine. On voit alors apparaître de part et d'autre de la ligne médiane, deux dépressions qui correspondront aux yeux
- L'organogénèse qui s'étend jusqu'à la fin de la 8ème semaine voit se développer les yeux de façon très avancée
- La différenciation des éléments oculaires en cristallin, rétine, cornée; etc. survient ensuite et se continue même après la naissance en ce qui concerne la région maculaire.
1) Jusqu'à la fin de la 3ème semaine (embryogénèse)
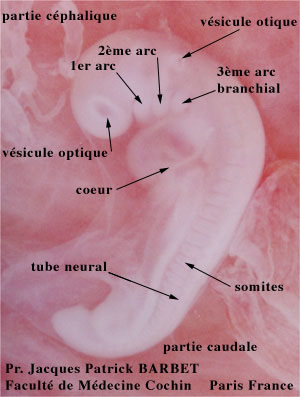
Embryon humain de 26 jours
Stade 12 Carnegie
La neurulation correspond à l'apparition, de chaque côté de l'axe crânio-caudal, de paires de somites mésodermiques qui sont des renflements alignés deux à deux. Elles délimitent la future colonne vertébrale. Latéralement, le mésoderme se divise en deux couches, l'une associée à l'ectoderme et l'autre à l'endoderme sous-jacent. Il y a 42paires de somites en tout. Les somites les plus proches du segment crânial donneront les éléments céphaliques.
Des cellules de la crête neurale vont migrer vers le mésoderme crânial. Certaines vont progresser sous l'ectoderme et une fois arrivées à destination, elles vont se multiplier, se différencier et participer à la création de l''orbite et de la face.
Les cellules de la crête neurale formeront le stroma cornéen et l'endothélium, le muscle ciliaire, le stroma uvéal et les mélanocytes, la plupart de la sclère, les gaines méningées et le tissu conjonctif du nerf optique. Au niveau de la face, ces cellules de la crête neurale vont donner les paupières, la conjonctive, l'orbite. Seuls l'endothélium des vaisseaux et les muscles striés ont comme origine le mésoderme paraaxial et les somites préotiques. Les péricytes des vaisseaux semblent provenir de la crête neurale.
A la fin de la troisième semaine la zone crâniale du tube neural montre trois renflements séparés par des sillons: ce sont les vésicules cérébrales primaires avec, d'avant en arrière, le prosencéphale, le mésencéphale et le rhombencéphale. Au même moment le développement de la partie postérieure du mésencéphale va donner la courbure du tube neural. Peu de temps après on note une seconde courbure plus postérieure, la courbure cervicale.
Plus tard encore, pendant la 4ème et la 5ème semaine, le prosencéphale se divise en télencéphale antérieur et diencéphale plus postérieur, et le rhombencéphale se divise en métencéphale antérieur, et myélencéphale, postérieur.
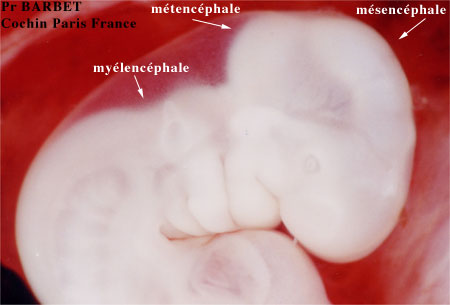
Embryon de 32 jours
L'ébauche des yeux apparaît vers le 22ème jour, comme 2 sillons de chaque côté de la ligne médiane à l'extrémité encore ouverte des plis neuraux antérieurs. Ces 2 sillons sont situés entre le télencéphale et le diencéphale et sont donc formés par l'invagination des plis neuraux. Cela va aboutir à la formation des gouttières optiques qui se transformeront en vésicules optiques.
Cette apparition des ébauches oculaires va terminer la phase de l'embryogénèse et laisser place à l'organogénèse.
2) La 4ème semaine (organogénèse)
Lorsque le neuropore se ferme le 24ème jour, les ébauches optiques se transforment en évagination du tube neural et deviennent les vésicules optiques. Ces vésicules sont en continuité avec le tube neural, les futurs ventricules cérébraux. La pression qui règne dans le liquide contenu dans le tube neural va permettre une expansion de ces vésicules optiques.
Les vésicules vont ainsi se développer et venir près de l'ectoderme. Une constriction va apparaître entre les vésicules et le tube neural.
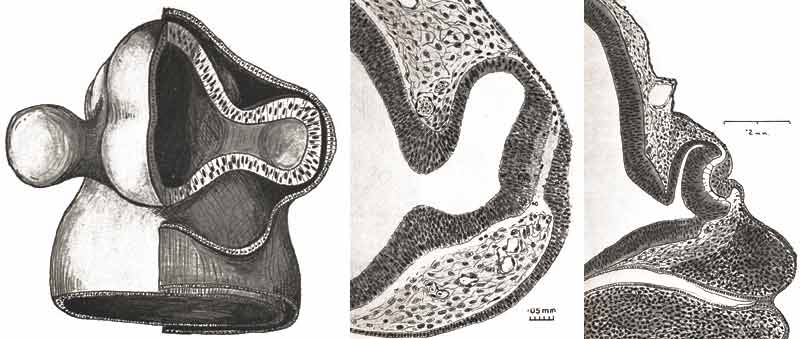
Développement des vésicules optiques et apparition de la placode cristallinienne
Ida Mann
Le 27ème jour, les cellules ectodermiques recouvrant la vésicule optique vont se transformer et deviennent la placode cristallinienne. La minceur de cette zone est causée par l'élongation des tissus et une augmentation des divisions cellulaires.
Le 28ème jour la zone de la vésicule optique qui touche l'ectoderme forme le disque rétinien. A ce stade les deux feuillets de la vésicule peuvent donner une rétine sensorielle ou une rétine pigmentée (épithélium pigmentaire) comme on l'a vu dans le paragraphe de génétique.
A la fin de la 4ème semaine le processus d'invagination va commencer et les vésicules optiques vont devenir des cupules optiques reliées au cerveau par le pédicule optique.
Cette invagination va se faire progressivement et va laisser une fente inférieure ouverte au niveau du nerf optique, c'est la fente colobomique. Normalement cette fissure doit se fermer, sinon on observera des anomalies congénitales plus ou moins graves, les colobomes.

Fermeture progressive de la fente colobomique inférieure
Hamilton et al. Human embryology 1972
La fissure embryonnaire permet la pénétration dans l'oeil de l'artère hyaloïde, branche de l'artère ophtalmique, et elle permet aussi l'extension du premier neurone (cellules visuelles) vers le diencéphale.
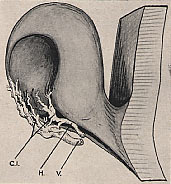
L'artère hyaloïde H située dans la fente colobomique
Ida Mann
A la fin de la quatrième semaine des vaisseaux vont recouvrir les cupules optiques. Les cellules de la zone de la cupule non invaginée (postérieures) sont au contact des vaisseaux et vont se pigmenter pour donner l'épithélium pigmenté de la rétine. Les cellules de la zone invaginée vont donner la rétine neuro-sensorielle.
Le mésenchyme périoculaire va se condenser pour former les muscles extrinsèques. Les muscles innervés par le nerf crânien III proviennent de la première paire de somites et apparaissent le 26ème jour. Le muscle moteur oculaire externe innervé par le nerf crânien VI provient du mésenchyme de la région maxilomandibulaire et apparaît le 27ème jour. Le muscle grand oblique provient de la deuxième paire de somites et apparaît le 29ème jour.
3) La 5 ème semaine
Cette période est dominée par l'invagination progressive de la cupule optique qui est rattachée à la partie antérieure du diencéphale par le canal neural.
L'invagination va entraîner l'oblitération de la cavité anciennement vésicule optique et cette cavité devient virtuelle, située entre la rétine neuro-sensorielle et l'épithélium pigmenté de la rétine. Elle pourra se recréer plus tard en cas de décollement de la rétine qui n'est qu'une séparation des deux feuillets rétiniens séparés dans les premiers stades du développement de l'oeil.
Le nerf optique va également se refermer progressivement.
Le 29ème jour l'invagination induit la formation de la placode cristallinienne qui n'était qu'un épaississement de l'ectoderme au contact de la vésicule optique. On assiste à l'arrêt des multiplications cellulaires au centre, et à une augmentation des divisions sur les bords de la placode.
La placode cristallinienne va s'enfoncer progressivement et devient la vésicule cristallinienne et se sépare de l'ectoderme petit à petit. Sa taille est assez importante et elle remplit une grande partie de la vésicule optique. Les cellules de la vésicule cristallinienne ont une orientation antéro-postérieure. La vésicule va se trouver entourée par des branches de l'artère hyaloïde. Cette artère, déjà présente dans la cupule optique, donne des branches qui vont atteindre le pôle postérieur de la vésicule cristallinienne. De l'autre côté, l'artère hyaloïde passe par la fente colobomique pour rejoindre les vaisseaux céphaliques.

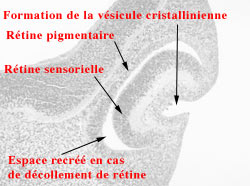
Invagination de la cupule optique au 26 ème jour (Stade 12 Carnegie)
Le vitré primitif se développe le long de l'artère hyaloïde.
La surface ectodermique, après séparation de la vésicule cristallinienne, va se différencier en une double couche de cellules, la cornée primitive.
A ce moment on assiste à la formation de la mandibule à partir du premier arc, et cela va concourir à la formation de l'orbite. Vers la fin de la cinquième semaine, les axes des deux orbites se tournent vers l'avant grâce à la croissance du maxillaire. A l'intérieur des orbites commencent à apparaître les muscles oculomoteurs.
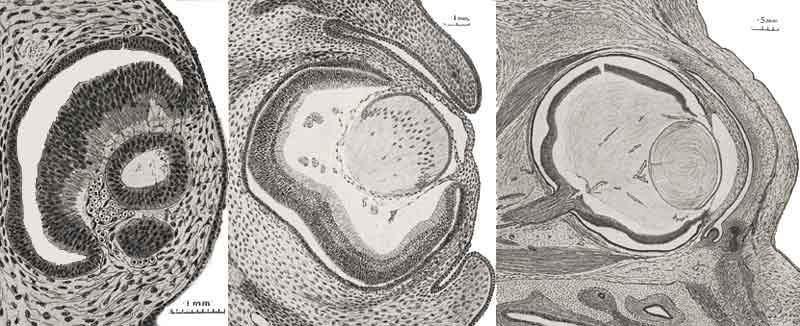
Transformation progressive de l'oeil
Images Ida Mann
4) La 6ème semaine
Cette période est marquée par de début de différenciation de l'épithélium pigmentaire rétinien, par la prolifération des cellules de la neuro-rétine, par la formation duvitré secondaire, par la transformation des cellules cristalliniennes postérieures en fibres primaires, par le développement des vaisseaux péri-oculaires et par l'apparition des paupières.

Embryon de 32 jours (Stade 14 Carnegie)
L'événement capital est la fermeture de la fente embryonnaire. Cette fermeture commence au milieu de la fente et va progresser vers l'avant et vers l'arrière. A la fin de la sixième semaine, on ne remarque qu'une encoche au niveau du bord antérieur et une quasi-fermeture en arrière, autour de l'artère hyaloïde.
L'épithélium pigmentaire existe en tant qu'une couche de cellules cubiques. La membrane basale de cet épithélium va être à l'origine d'une membrane de Bruch primitive. La rétine sensorielle s'amincit progressivement.
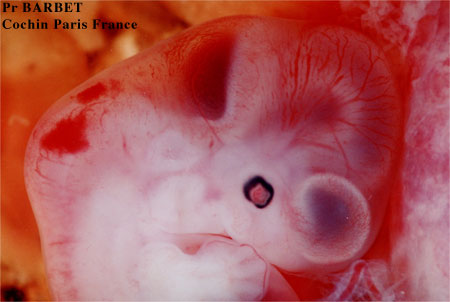
Embryon de 41 jours (Stade 17 Carnegie)
L'épithélium rétinien pigmentaire noir est visible
Le vitré primitif est formé, fortement attaché au cristallin, à la rétine et au futur disque optique. La fin de la sixième semaine voit apparaître les fibrilles du vitré secondaire à la face interne de la rétine sensorielle. Ce nouveau vitré pousse le vitré primitif vers l'avant et le détache de la rétine.
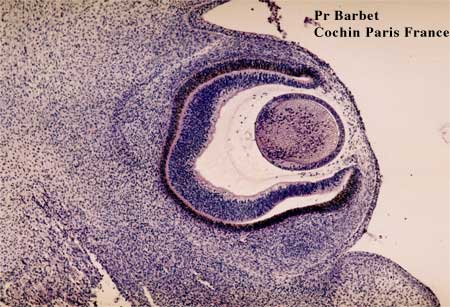
Coupe histologique à 41 jours
Les cellules de la cornée établissent des jonctions entre elles.
Les cellules du cristallin s'allongent pour remplir la cavité cristallinienne et se transformer ainsi en fibres cristalliniennes à la direction antéro-postérieure. Ce sont les fibres cristalliniennes primaires.
Les cellules antérieures du cristallin gardent l'aspect de cellules épithéliales. Un anneau germinatif de cellules très actives apparaît autour de la région centrale. Les cellules filles de cette région se déplacent vers la région équatoriale du cristallin, zone dans laquelle elles vont s'allonger et se différencier en cellules cristalliniennes secondaires. Elles forment des couches concentriques autour des fibres primaires du noyau cristallinien.
L'endroit où les fibres secondaires des points opposés de l'équateur se rejoignent correspond aux sutures cristalliniennes antérieures et postérieures.
Ainsi les fibres près de la périphérie sont les plus jeunes. Le cristallin va évoluer en apposant de nouvelles couches de fibres sur les plus anciennes.
Les fibres primaires et secondaires perdent leurs mitochondries et leur noyau cellulaire, progressivement.
En dehors des cataractes, on décrit différentes anomalies, les ectopies cristalliniennes, les lenticônes, les microsphérophakies et les aphakies.

Cristallin (grossissement de la coupe histologique à 41 jours)
Dans l'orbite, les premières myofibrilles apparaissent pour donner progressivement les muscles oculomoteurs. Le ganglion ciliaire fait son apparition dans l'orbite. Les vaisseaux se modifient pour créer les artères ciliaires postérieures.
La face se modifie nettement car les paupières apparaissent. La paupière supérieure provient de la formation fronto nasale et l'inférieure du bourgeon maxillaire.
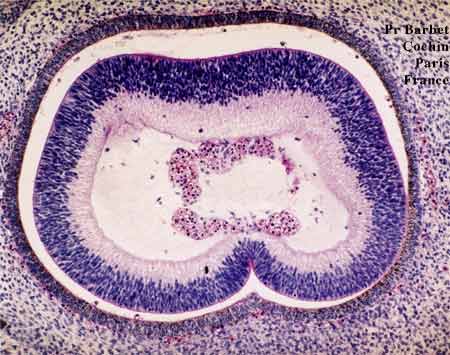
Coupe frontale à 44 jours (Stage 18 Carnegie)
Des éléments sanguins figurés siègent au centre
on aperçoit encore l'encoche inférieure (fermeture de la fente)

Section frontale du nerf optique
avec la fermeture inférieure de la fente colobomique
En haut, cellules pigmentées rétiniennes
5) La 7ème semaine
La fermeture de la fente colobomique est complète dès les premiers jours de cette semaine de développement.
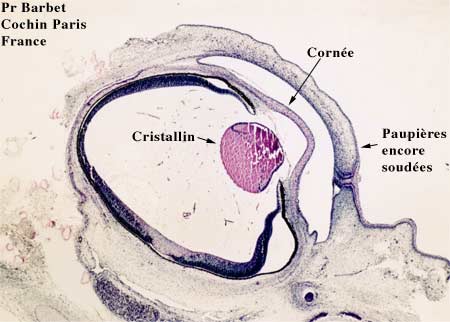
Coupe de l'oeil à 12 semaines
La rétine poursuit son développement puisque les cellules de l'épithélium pigmentaire forment une couche unicellulaire de cellules cubiques et on voit apparaître à l'intérieur des mitochondries, du réticulum endoplasmique, des ribosomes et des promélanosomes. Ces derniers vont se transformer progressivement en mélanosomes qui donneront l'aspect pigmenté de cet épithélium.
Le neuro-épithélium va lui aussi se transformer petit à petit pour voir apparaître les cellules visuelles, cônes et bâtonnets.
Le cristallin est rempli par les cellules postérieures qui se sont allongées au maximum et vont remplir la vésicule cristallinienne. Ces cellules vont perdre leurs organelles cytoplasmiques et acquérir un matériel fibrillaire. Ce seront alors les fibres cristalliniennes primitives, correspondant au futur noyau cristallinien embryonnaire.
Le vitré se développe, avec l'apparition de cellules de collagène de type I, solides autour de la papille et au niveau de la périphérie rétinienne.
Cette période marque surtout le développement du mésenchyme périoculaire, avec la création de la chorio-capillaire.
La théorie de Tripathi décrit l'évolution du mésenchyme en trois phases. Des cellules de la crête neurale vont donner une première vague de mésenchyme qui va se situer entre la surface de l'ectoderme et le cristallin pour donner l'endothélium cornéen et trabéculaire. La deuxième vague va se placer entre l'épithélium cornéen primitif et l'endothélium, pour former les kératocytes et le stroma cornéen. La troisième vague va se situer entre le cristallin et l'endothélium cornéen pour se transformer en stroma irien.
On voit apparaître également, à partir d'un anneau irien externe (grand cercle vasculaire de l'iris), des vaisseaux qui pénètrent le stroma irien.

Coupe de l'oeil à 16 semaines
L'épithélium pigmenté rétinien semble induire la formation de la sclère à partir de mésenchyme périoculaire. Il y aura une condensation progressive des fibres, pour aboutir à un tissu résistant.
Les cellules mésenchymateuses vont aussi beaucoup s'allonger pour former les muscles oculomoteurs.
6) La 8ème semaine
On assiste à la maturation de l'épithélium pigmentaire, avec une augmentation du nombre des prémélanosomes et des mélanosomes contenus dans les cellules.
La rétine neuro-sensorielle se différencie de mieux en mieux en différentes couches. Dans la couche interne, les cellules ganglionnaires envoient leur axones vers la papille qui va devenir progressivement la papille de Bergmeister qui est composée des axones et des cellules gliales qui ont proliféré.
Au cours de cette période, le système hyaloïde vasculaire est tout à fait formé. Le vitré secondaire va se développer autour du vitré primaire et autour du système hyaloïde. Les artères ciliaires longues postérieures ayant atteint le corps ciliaire s'anastomosent avec les vaisseaux annulaires.
La différenciation se poursuit dans la cornée. L'endothélium est alors formé d'une double couche de cellules cubiques et font former la membrane de Descemet, qui semble formée par un épaississement.
7) Le troisième mois
La différenciation de la rétine se précise rapidement, Elle se propage des couches les plus internes de la rétine, vers les couches les plus externes et en particulier lesphotorécepteurs, cônes et bâtonnets. Elle progresse également du pôle postérieur, vers l'avant, donc vers la périphérie de la rétine.
Le nerf optique se modifie assez rapidement aussi. Une fine membrane gliale recouvre la partie antérieure de la papille, c'est la papille de Bergmeister, puis elle disparaît progressivement. On commence à voir des lacunes au sein des fibrilles, avant leur disparition.
Le mésenchyme péri-oculaire va suivre le développement de l'oeil. La choriocapillaire se forme, ainsi que les vaisseaux du corps ciliaire et de l'iris.
Le cristallin continue sa transformation et devient ovale, à cause de la prolifération continue des cellules équatoriales. On peut alors déceler un noyau embryonnaire, sans suture, et dû à l'élongation des fibres des cellules cristalliniennes postérieures, et un noyau foetal présentant des sutures et formé par la prolifération équatoriale.
La cornée se différencie progressivement et voit apparaître des cellules à desmosomes attachées aux cellules sous-jacentes. Le collagène du stroma apparaît. Cette cornée déjà opalescente et bientôt transparente va changer nettement de courbure. La chambre antérieure se forme entre l'endothélium cornéen et l'iris.
Les paupières se soudent et ne s'ouvriront que beaucoup plus tard. Les cellules des glandes lacrymales se forment. Les muscles oculomoteurs se forment et sont attachés sur la sclère.
8) Le quatrième mois
La rétine est quasiment terminée et commence à être vascularisée.
C'est l'époque où le système hyaloïde va régresser. Le grand cercle artériel de l'iris se forme. Le vitré tertiaire apparaît et va donner la zone de Zinn qui suspend le cristallin.
Le cristallin s'amincit et la cornée continue sa maturation. Son épithélium est encore formée de deux assises de cellules.
La sclère est bien formée. Dans l'orbite les muscles oculomoteurs se soudent progressivement avec les tendons.
9) Le cinquième mois
Il est caractérisé par la différenciation des photorécepteurs de la rétine.
La vascularisation rétinienne progresse régulièrement.
Au fil des mois suivants, la maturation des différents tissus va progresser et en particulier la rétine.
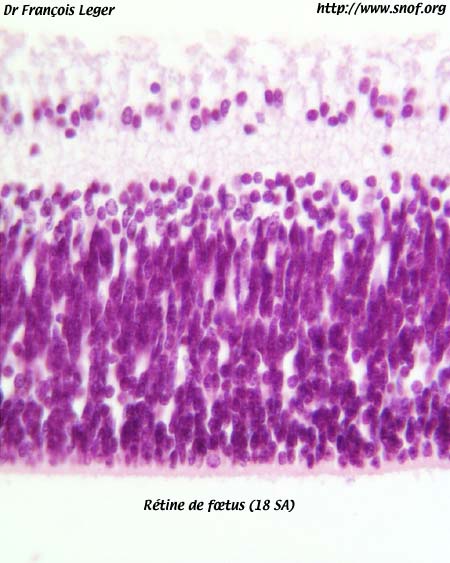
10) Après la naissance
Le développement de l'oeil peut être considéré comme terminé, en dehors de la maturation de la macula. On assiste à une concentration des cônes sur la macula, de 18 pour 100µm lors de la première semaine après la naissance, jusqu'à 42 pour 100µm à l'âge adulte. Ceci va se faire parallèlement à la croissance des synapses cérébrales.
Bibliographie
Un des (très) rares livres sur le sujet:
Y.Robert Barishak Embryology of the Eye and its Adnexae
Conclusion
Nous allons essayer de compléter ce chapitre au fil du temps, car on assiste tous les jours à des progrès dans la connaissance de la formation embryonnaire. Lesmécanismes génétiques ne sont que très mal connus actuellement, et leur étude nous fait progressivement prendre conscience de l'immensité de notre ignorance.

Visage d'enfant
Domenico Ghirlandajo















































































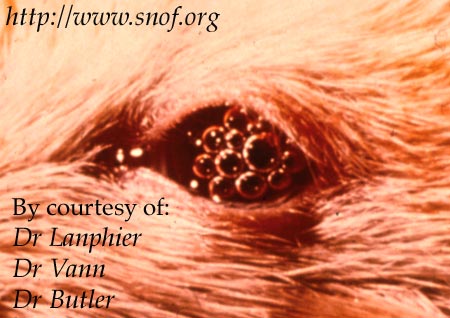

 Kératocône (keratoconus)
Kératocône (keratoconus)
